题目内容
4. 如图表示的是地壳里所含各种元素的质量分数.请根据如图回答下列问题:
如图表示的是地壳里所含各种元素的质量分数.请根据如图回答下列问题:(1)图中表示金属元素6种;
(2)硅的工业制备原理SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO,反应前后化合价变化变化最大的元素是硅元素;
(3)地壳中含量最多的非金属元素与含量最多的金属元素之间,能形成一种氧化物.此氧化物硬度极大,俗称刚玉,这种氧化物的化学式为Al2O3.
分析 (1)根据地壳里所含各种元素的质量分数图,找出金属元素;
(2)根据化合价原则计算元素的化合价进行分析;
(3)根据地壳里所含各种元素的质量分数图,查出地壳中含量最多的非金属元素和含量最多的金属元素,写出形成氧化物的化学式.
解答 解:(1)由地壳里所含各种元素的质量分数图可知,图中表示出的金属元素有铝、铁、钙、钠、镁6种;
(2)由硅的工业制备原理为SiO2+2C $\frac{\underline{\;高温\;}}{\;}$ Si+2CO↑,可知:硅元素由+4价降到0价,氧化合价不变,碳化合价由0价升到+2价,故反应前后化合价变化最大的元素是:硅元素;
(3)由地壳里所含各种元素的质量分数图可知,地壳中含量最多的非金属元素是氧,含量最多的金属元素是铝,二者形成的氧化物是氧化铝,化学式是:Al2O3.
故答为:(1)6;(2)硅元素;(3)Al2O3.
点评 本题比较简单,属于基础知识的题型,应加强基础知识的学习.

练习册系列答案
相关题目
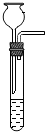
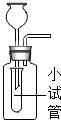
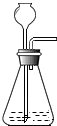
12.被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的双氧水(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.在化学实验开放日,实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体,请填写有关内容:
(1)B试管中发生反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?用带火星木条放在试管口,木条复燃,证明产生的气体是氧气.
(3)该实验加入少量二氧化锰,其作用是催化作用.
| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象.  | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是: 水; B试管中的无色液体是: 过氧化氢; |
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?用带火星木条放在试管口,木条复燃,证明产生的气体是氧气.
(3)该实验加入少量二氧化锰,其作用是催化作用.
19.下列有关溶液的说法中,正确的是( )
| A. | 溶液都是澄清、透明、无色的 | |
| B. | 溶液都是由溶质和溶剂混合而成的 | |
| C. | 只有水才能做溶剂 | |
| D. | 所有物质的溶解度都是随温度的升高而增大的 |
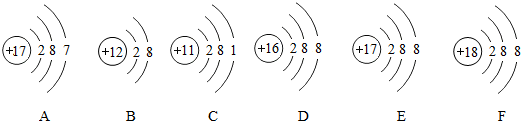
13.下列粒子结构示意图表示阳离子的是( )
| A. |  | B. | 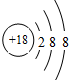 | C. | 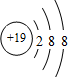 | D. | 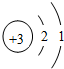 |