题目内容
2.8g某化合物在空气中完全燃烧后共生成8.8g CO2和3.6g H2O,则该化合物的组成可能是( )
| A、CH4 |
| B、C2H4 |
| C、C2H4O2 |
| D、C3H6 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据题意“2.8g某物质在氧气中完全燃烧,生成8.8g二氧化碳和3.6g水”及质量守恒定律反应前后元素的质量及种类不变可知,该物质一定含有碳、氢元素,可能含有氧元素.再根据二氧化碳的碳元素、水中氢元素的质量的和与1.6g的关系,判定氧元素的存在情况;最后根据各元素的质量和相对原子质量推出可能的化学式.
解答:解:
由质量守恒定律反应前后元素的种类不变,确定:该物质中一定含有碳、氢两种元素,可能含有氧元素.再根据反应前后元素的质量相等,来确定氧元素是否含有.8.8g二氧化碳中碳元素的质量为:8.8g×
×100%=2.4g,3.6g水中氢元素的质量为:3.6g×
×100%=0.4g.2.4g+0.4g=2.8g与原物质的质量相等,故一定不含氧元素.碳、氢元素的原子个数比为:
:
=1:4,所以,可能的化学式是:CH4.
故选:A.
由质量守恒定律反应前后元素的种类不变,确定:该物质中一定含有碳、氢两种元素,可能含有氧元素.再根据反应前后元素的质量相等,来确定氧元素是否含有.8.8g二氧化碳中碳元素的质量为:8.8g×
| 12 |
| 44 |
| 2 |
| 18 |
| 2.4g |
| 12 |
| 0.4g |
| 1 |
故选:A.
点评:本题是运用化学中的基本思想质量守恒思想,学会处理此类计算的题目,从而培养了学生的创新思维能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列生活物品中,用有机合成材料制作的是( )
A、 铁锅 |
B、 乳胶手套 乳胶手套 |
C、 不锈钢餐具 |
D、 瓷器 |
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
则该密闭容器中发生反应的说法正确的是( )
则该密闭容器中发生反应的说法正确的是( )
| 物质 | X | Y | Z | Q |
| 反应前质量(g) | 3l | 8 | 2 | 5 |
| 反应后质量(g) | M | 1 | 42 | 3 |
| A、属于化合反应 |
| B、分解反应 |
| C、置换反应 |
| D、M的数字是0 |
正确的操作是实验成功的关键之一,以下操作正确的是( )
A、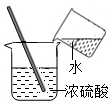 稀释浓硫酸 稀释浓硫酸 |
B、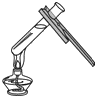 加热液体 |
C、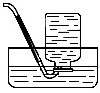 收集气体 |
D、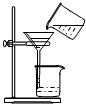 过滤 |
下列化学实验操作正确的是( )
A、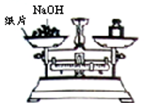 称量氢氧化钠固体 |
B、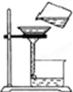 过滤 |
C、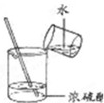 稀释浓硫酸 |
D、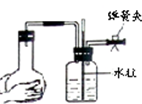 检查装置气密性 |
如图四位同学正在讨论某一个化学方程式表示的意义,根据他们描述的内容,试判断他们所指的化学方程式是( )


A、S+O2
| ||||
B、2CO+O2
| ||||
C、2H2+O2
| ||||
D、CH4+2O2
|
下列关于水的说法中,正确的是( )
| A、水中氢元素与氧元素的质量比为2:1 |
| B、水是由氢、氧两种原子组成的化合物 |
| C、水是由氢气和氧气组成的 |
| D、水被电解时所发生的反应是分解反应 |
下列关于原子的叙述中,正确的是( )
| A、是不能再分的粒子 |
| B、都是由质子和中子构成的 |
| C、不能直接构成物质 |
| D、是化学变化中的最小粒子 |
要从高锰酸钾加热完全分解后的剩余物中回收二氧化锰固体,有下列操作可选择:
①过滤;②烘干;③加水溶解;④洗涤固体;⑤蒸发结晶.其操作顺序正确的是( )
①过滤;②烘干;③加水溶解;④洗涤固体;⑤蒸发结晶.其操作顺序正确的是( )
| A、①②③④ | B、③①④② |
| C、③②①⑤ | D、③①⑤④ |