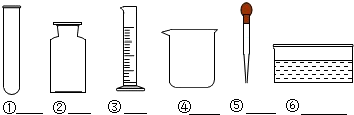
题目内容
20.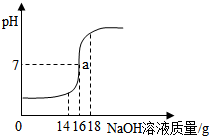 将5%的NaOH溶液逐滴加入73g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.
将5%的NaOH溶液逐滴加入73g稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.试回答:
(1)a点溶液中大量存在的离子有钠离子和氯离子.
(2)当恰好完全反应时,消耗NaOH溶液的质量为16g.
(3)计算稀盐酸中溶质的质量分数.
分析 (1)a点时,溶液的pH等于7,说明稀盐酸和氢氧化钠恰好完全反应生成氯化钠和水,溶液中大量存在的离子是钠离子和氯离子;
(2)根据图中信息可以判断当恰好完全反应时,消耗NaOH溶液的质量;
(3)根据氢氧化钠溶液质量、溶质质量分数可以计算氯化氢的质量,进一步可以计算稀盐酸中溶质的质量分数.
解答 解:(1)a点溶液中大量存在的离子有钠离子和氯离子.
故填:钠离子和氯离子.
(2)当恰好完全反应时,消耗NaOH溶液的质量为16g.
故填:16g.
(3)设稀盐酸中氯化氢的质量为x,
NaOH+HCl═NaCl+H2O,
40 36.5
16g×5% x
$\frac{40}{16g×5%}$=$\frac{36.5}{x}$,
x=0.73g,
稀盐酸中溶质的质量分数为:$\frac{0.73g}{73g}$×100%=1%,
答:稀盐酸中溶质的质量分数为1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
8.水冷却后,除了会凝固成冰晶体外,还会形成玻璃态,它是由液态水急速冷却到-108℃时形成的,玻璃态水与普通水密度相同,下列有关说法错误的是( )
| A. | 水冷却到0℃时形成的冰水混合物是纯净物 | |
| B. | 水结冰后分子间距离不变 | |
| C. | 水由液态变为玻璃态体积不变 | |
| D. | 水变为冰或玻璃态均属于物理变化 |
15.现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验:
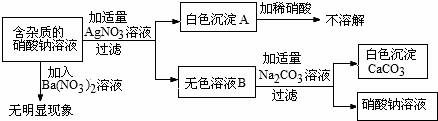
下列判断正确的是( )

下列判断正确的是( )
| A. | 原溶液中的杂质可能由三种物质组成 | |
| B. | 原溶液中的杂质一定是氯化钙 | |
| C. | 无色溶液B的溶质是硝酸钙 | |
| D. | 该实验中涉及的基本反应类型不止一种 |
12.我们盘锦地区使用的粗盐大多由海水为原料制得的,其中除了含有泥沙等难溶性物质外还含有一些可溶性钙镁化合物,如氯化钙,氯化镁等.几位同学想除去粗盐中难溶性杂质,并对所得精盐的成分进行研究.请你帮助他们完成设计方案:
(1)除去粗盐中难溶性杂质:操作步骤如下:①溶解,②过滤,③蒸发,④回收并计算产率.此过程中都用到的玻璃仪器是玻璃棒,它在步骤③中的作用是搅拌防止局部温度过高造成液体飞溅.
(2)在上述除杂质采用的方法中利用了氯化钠的溶于水和溶解度受温度影响较小性质.
(3)在制得的精盐中除了含有氯化钠外还含有氯化钙,氯化镁等,检验方案如下:
(1)除去粗盐中难溶性杂质:操作步骤如下:①溶解,②过滤,③蒸发,④回收并计算产率.此过程中都用到的玻璃仪器是玻璃棒,它在步骤③中的作用是搅拌防止局部温度过高造成液体飞溅.
(2)在上述除杂质采用的方法中利用了氯化钠的溶于水和溶解度受温度影响较小性质.
(3)在制得的精盐中除了含有氯化钠外还含有氯化钙,氯化镁等,检验方案如下:
| 实验目的 | 实验步骤 | 实验现象 | 实验结论 |
检验精盐中的物质 | 取少量精盐加水溶解: ①加入碳酸钠溶液; ②另取样加入氢氧化钠溶液 | 都产生 白色沉淀. | ①含有氯化钙 ②含有氯化镁 |
10.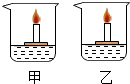 烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )
烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )
 烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )
烧杯中分别盛有两种溶质不同的无色溶液,小木块上各有一支燃着的蜡烛,向甲烧杯撒入白色粉末X后,发现烧杯中蜡烛会熄灭,向乙烧杯中撒入黑色粉末Y后,则发现烧杯中蜡烛燃烧更旺.根据所学知识推测,X、Y分别是( )| A. | X:Al(OH)3 Y:C | B. | X:Mg Y:CuO | ||
| C. | X:Na2CO3 Y:MnO2 | D. | X:CaCO3 Y:Fe3O4 |