题目内容
15.下列净化水的操作中,单一操作相对净化程度较高的是( )| A. | 吸附沉淀 | B. | 静置沉淀 | C. | 过滤 | D. | 蒸馏 |
分析 根据常见的净化水的方法和原理,对比分析,判断净化程度最高的方法.
解答 解:
A、通过沉降可使水中悬浮的大颗粒固体沉降,所得到的水中可能还会含有小颗粒的固体及可溶性杂质,净化程度不高.
B、静置沉淀,所得到的水中可能还会含有小颗粒的固体及可溶性杂质,净化程度不高.
C、通过过滤而除去了水中不溶性固体杂质,但对于可溶性杂质过滤并不能除去,所得到的水中仍含有可溶性杂质,净化程度不能达到最高.
D、通过蒸馏除去了水中所有的杂质,所得到的水为纯净物,净化程度最高
故选:D.
点评 净化水通常所采取的沉降、吸附、过滤、消毒杀菌、煮沸、蒸馏等操作中,由于蒸馏后所得到的水为纯净物,因此净化程度最高.

练习册系列答案
相关题目
6.小李喜欢化学,下列是他平时的部分观察、记录、分析、总结,其中不科学的是( )
| A. | 削皮苹果未及时吃掉,露置于空气中一段时间后“生锈”,是氮气作祟 | |
| B. | 灼烧聚乙烯塑料和聚氯乙烯塑料时,聚氯乙烯会生成刺激性气味的气体 | |
| C. | 家用不粘锅涂层的主要成分是聚四氟乙烯(C2F4)n,聚四氟乙烯是有机高分子合成材料 | |
| D. | 家用一次性纸杯,倒入开水而不被水浸渍烂掉,是因为纸杯为复合材料 |
3.下列关于化学反应“X2+3Y2=2Z”的叙述错误的是( )
| A. | Z的化学式为XY3 | |
| B. | 若mgX2和ngY2恰好完全反应,则生成(m+n)gZ | |
| C. | 若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N) | |
| D. | 若ag X2完全反应生成bg Z,则同时消耗(b-a) g Y2 |
20.下列反应中,属于分解反应的是( )
| A. | 酒精+氧气 $\stackrel{点燃}{→}$ 二氧化碳+水 | B. | 氢气+氧气 $\stackrel{点燃}{→}$ 水 | ||
| C. | 氧化汞 $\stackrel{加热}{→}$ 汞+氧气 | D. | 乙炔+氧气 $\stackrel{点燃}{→}$二氧化碳+水 |
7.在氧气中燃烧生成黑色固体的是( )
| A. | 木炭 | B. | 蜡烛 | C. | 铁丝 | D. | 红磷 |
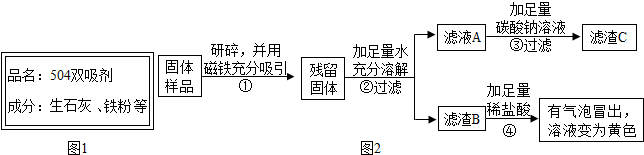
4.红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图1所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3,久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究1】甲同学的方案:
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙和水反应生成氢氧化钙,也能使酚酞试液变红.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
【实验探究2】乙、丙同学设计如下实验方案继续验证:
(1)③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)乙、丙同学实验中又能得出固体样品中一定还含有Fe2O3,仍有一种物质不能确定,该物质是Ca(OH)2.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3,久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)CaO+H2O═Ca(OH)2.
【实验探究1】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液. | 固体溶解时试管外壁发烫,试管底部有不容物,溶液变红. | 固体中一定含有CaO 多余和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀HCl. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙和水反应生成氢氧化钙,也能使酚酞试液变红.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
【实验探究2】乙、丙同学设计如下实验方案继续验证:
(1)③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)乙、丙同学实验中又能得出固体样品中一定还含有Fe2O3,仍有一种物质不能确定,该物质是Ca(OH)2.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.

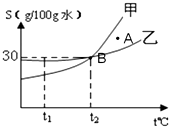 如图是甲、乙两种物质的溶解度曲线.
如图是甲、乙两种物质的溶解度曲线.