题目内容
8.硝酸铵(NH4NO3)是一种常用化肥,计算(1)NH4NO3的相对分子质量
(2)NH4NO3中氮、氢、氧元素的质量比
(3)NH4NO3中氮元素的质量分数.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(3)根据化合物中元素质量分数的计算方法来分析解答.
解答 解:(1)硝酸铵的相对分子质量是14×2+1×4+16×3=80.故填:80;
(2)硝酸铵中氮、氢、氧三种元素之间的质量之比是(14×2):(1×4):(16×3)=7:1:12.故填:7:1:12;
(3)NH4NO3中氮元素的质量分数为:$\frac{14×2}{80}×100%$=35%;故填:35%.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
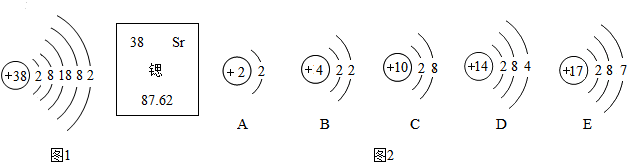
18.下列物质中直接由原子构成的是( )
| A. | 氮气 | B. | 铁 | C. | 二氧化硫 | D. | 四氧化三铁 |
19.正确的实验操作能保证化学实验的顺利进行.下列实验操作不正确的是( )
| A. | 点燃可燃性的气体之前要先验纯 | |
| B. | 用量筒量取一定量的液体时,视线应与液面最低处相齐 | |
| C. | 加热高锰酸钾制取氧气,用排水法收集完氧气,先将导管移出水面,后停止加热 | |
| D. | 将氢氧化钠固体直接放在托盘天平的托盘上称量 |
16.某工地发生多人食物中毒,经化验为误食工业用盐(NaNO2)所致,NaNO2中氮元素的化合价是( )
| A. | +2 | B. | +4 | C. | +3 | D. | +5 |
20.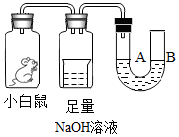 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )| A. | A处上升,B处下降 | B. | A、B两处都下降 | C. | A处下降,B处上升 | D. | A、B两处都不变 |
17.锅炉烧煤时用鼓风机将煤粉吹起,形成沸腾状燃烧.其目的是( )
| A. | 可以降低煤的着火点 | |
| B. | 可以减少有害气体的产生 | |
| C. | 可以使煤成为绿色燃料 | |
| D. | 能增加与氧气的接触面积,能使煤充分燃烧 |
18.一块质量为4克的合金,与足量的盐酸反应完全后生成氢气0.2克,则该合金可能是( )
| A. | 铁镁 | B. | 铁铜 | C. | 铁锌 | D. | 镁铝 |