题目内容
1.某兴趣小组欲测定当地石灰石中碳酸钙的纯度,称取200g石灰石样品和一定量的稀盐酸恰好完全反应(其中杂质不参加反应),完全反应后测得剩余物质的质量减少44g,求石灰石中碳酸钙的质量分数?分析 根据该反应中只有二氧化碳是气体,则利用质量守恒定律和反应前后减少的质量即为二氧化碳的质量;将二氧化碳的质量代入化学反应方程式来计算碳酸钙的质量,再计算碳酸钙的质量分数.
解答 解:由质量守恒可知,二氧化碳的质量为44g,
设碳酸钙的质量为x.
则CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 44g
$\frac{100}{x}=\frac{44}{44g}$
解得x=100g
该石灰石中碳酸钙的质量分数为$\frac{100g}{200g}$×100%=50%.
点评 本题考查学生利用化学反应方程式的计算,明确二氧化碳是气体并利用质量守恒来计算二氧化碳的质量是解答的关键.

练习册系列答案
相关题目
13.下列有关叙述错误的是( )
| A. | 实验用剩的药品不能放回原试剂瓶 | |
| B. | 空气的主要成分是氮气和氧气 | |
| C. | 向试管中滴加液体,滴管应垂悬试管口上方 | |
| D. | 造成空气污染的主要气体有CO、CO2和SO2 |
10.生活中的下列物质,属于纯净物的是( )
| A. | 矿泉水 | B. | 葡萄酒 | C. | 水银 | D. | 澄清石灰水 |
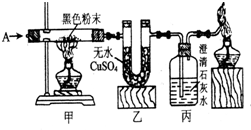 按如图进行实验,已知A为H2、CO中的一种或两者的混合物,甲装置中的黑色粉末为CuO、炭粉中的一种或两者的混合物.
按如图进行实验,已知A为H2、CO中的一种或两者的混合物,甲装置中的黑色粉末为CuO、炭粉中的一种或两者的混合物.