题目内容
10.请结合所学知识回答下列问题:(1)我国第五套人民币硬币铸造用到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:
Ni+H2SO4═NiSO4+H2↑,Fe+NiCl2═Ni+FeCl2,这两个反应的基本类型都是置换反应.四种金属活动性由强到弱的顺序为Al>Fe>Ni>Cu(用元素符号表示).
(2)在硫酸铜、硫酸锌和稀硫酸的混合溶液中,加入一定量的铁粉,使之充分反应后铁有剩余,过滤,滤液中一定含有ZnSO4、FeSO4(填化学式).
分析 (1)根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来进行分析;
(2)根据在金属活动性顺序中,只有氢前的金属可以和稀酸溶液反应生成氢气,只有排在前面的金属可以把排在它后面的金属从它的盐溶液中置换出来(钾、钙、钠除外)进行分析.
解答 解:(1)这两个反应都是一种单质和一种化合物生成一种单质和一种化合物的反应,属于置换反应;Ni+H2SO4═NiSO4+H2↑,说明Ni>H;Fe+NiCl2═Ni+FeCl2,说明Fe>Ni,所以这四种金属的活动性顺序为:Al>Fe>Ni>Cu;
(2)金属活动性顺序为:锌>铁>氢>铜,由于铁在氢和铜的前面,因此铁可以和硫酸铜溶液和稀硫酸反应,而铁不与硫酸锌反应,由于铁有剩余,说明能够和铁发生反应的物质都被消耗完毕,因此滤液中一定没有硫酸铜和硫酸;由于铁和硫酸铜反应能生成金属铜,因此滤渣中一定含有生成的金属铜和剩余的铁.
故答案为:(1)置换反应,Al>Fe>Ni>Cu.
(2)ZnSO4、FeSO4.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案
相关题目
3.镍(Ni)是一种不常见的金属,为了检测铁和镍(Ni)的金属活动性,小明同学在老师的指导下做了实验,结果如下表:
则它们的金属活动性顺序为( )
| 项目 | HCl溶液 | Fe的盐溶液 | Ni的盐溶液 |
| Fe | 有气体生成 | - | 有金属析出 |
| Ni | 有气体生成 | 无金属析出 | - |
| A. | Fe>Ni>H | B. | H>Ni>Fe | C. | Fe>H>Ni | D. | Ni>Fe>H |
5.石墨烯是从石墨材料中剥离制得,与金刚石、石墨一样,都只有碳元素组成.如图是金刚石、石墨、C60和石墨烯的微观结构示意图.下列说法正确的是( )
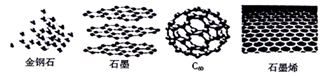

| A. | 它们都是由分子构成的 | |
| B. | 一个C60分子由60个碳原子构成 | |
| C. | 它们的结构中碳原子的排列方式都相同 | |
| D. | 它们的物理性质相同,化学性质不同 |
15.下列化学反应可用如图表示的是( )
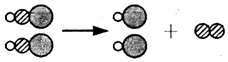

| A. | H2CO3 $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+H2O | B. | 2H2SO3+O2═2H2SO4 | ||
| C. | 2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑ | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
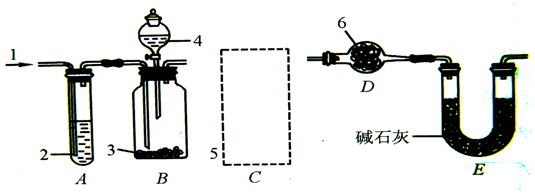
2.石灰石是制造水泥、石灰、轻质碳酸钙的主要原料来源.某校科学探究小组同学把一块从山中捡来的石灰石做纯度分析,进行了如下实验:他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(反应生成的氯化钙能溶于水,杂质不溶于水,也不与盐酸反应).(化学方程式如下:CaCO3+2HCl═CaCl2+H2O+CO2↑)
请计算:
(1)样品中的碳酸钙的质量分数是多少?
(2)上表中的m=3
(3)整个实验过程中共生成二氧化碳的质量为多少?
(4)高温加热10g纯净的碳酸钙,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%.计算反应生成的二氧化碳是多少克?(化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑)
| 序 号 | 第一次 | 第二次 | 第三次 | 第四次 |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体质量(g) | 5.5 | m | 1.6 | 1.6 |
(1)样品中的碳酸钙的质量分数是多少?
(2)上表中的m=3
(3)整个实验过程中共生成二氧化碳的质量为多少?
(4)高温加热10g纯净的碳酸钙,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%.计算反应生成的二氧化碳是多少克?(化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑)
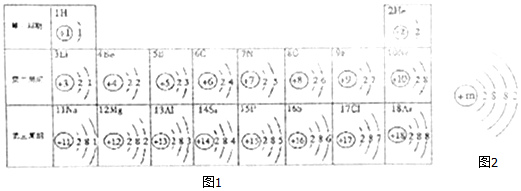
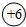 表示核内带6个单位正电荷,
表示核内带6个单位正电荷,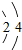 表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.
表示核外有6个电子,分两层排布,通常最外层电子数为8时较稳定.