题目内容
18.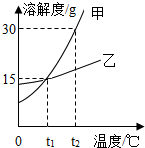 如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:
如图为甲、乙两种固体物质的溶解度曲线,请根据图示回答下列问题:(1)在t1℃时,甲、乙两物质的溶解度相等;
(2)t2℃时,将20g甲投入到50g水中,充分搅拌后所得溶液的质量为65g;
(3)将t2℃时甲物质的饱和溶液降温至t1℃,溶液中溶质的质量分数减小(填“增大”、“减小”或“不变”);
(4)要使接近饱和的乙溶液转化为饱和溶液,可以采用的一种方法是增加溶质.
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;在t1℃时,甲、乙两物质的溶解度相等;t2℃时,甲的溶解度是30g,因此将20g甲投入到50g水中,充分搅拌后所得溶液的质量=15g+50g=65g;将t2℃时甲物质的饱和溶液降温至t1℃,溶液中溶质的质量分数减小,因为降温后A的溶解度变小了;要使接近饱和的乙溶液转化为饱和溶液,可以采用的方法是:增加溶质,蒸发溶剂,降低温度.
解答 解:(1)由溶解度曲线可知:在t1℃时,甲、乙两物质的溶解度相等;故答案为:t1;
(2)t2℃时,甲的溶解度是30g,因此将20g甲投入到50g水中,充分搅拌后所得溶液的质量=15g+50g=65g;故答案为:65;
(3)将t2℃时甲物质的饱和溶液降温至t1℃,溶液中溶质的质量分数减小,因为降温后A的溶解度变小了;故答案为:减小;
(4)要使接近饱和的乙溶液转化为饱和溶液,可以采用的方法是:增加溶质,蒸发溶剂,降低温度;故答案为:增加溶质(合理即可)
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算、饱和溶液与不饱和溶液的转化等,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
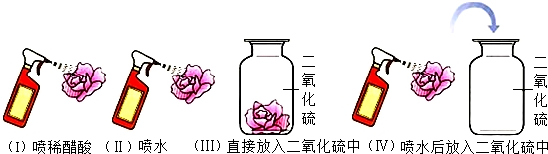
4.甲乙丙丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液,溶液变成了红色,一会儿红色就消失了.
【猜想】甲:可能是酚酞变质的缘故; 乙:可能是NaOH溶液与空气中CO2反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;丁:可能与氢氧化钠溶液质量分数大小有关.
【查阅资料】:碳酸钠溶液显碱性.
【理论分析】:
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是:若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象.
(2)乙同学的猜想也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试剂变红.
【实验设计】
(3)为证实丙同学的猜想,还需作如下实验,请完成如表:
(4)通过以上实验,四位同学看到:溶液先变成红色,一会儿红色又消失.因此酚酞红色褪去与氧气无关.若丁同学的猜想正确,设计如下实验证明并完成有关问题:
【猜想】甲:可能是酚酞变质的缘故; 乙:可能是NaOH溶液与空气中CO2反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;丁:可能与氢氧化钠溶液质量分数大小有关.
【查阅资料】:碳酸钠溶液显碱性.
【理论分析】:
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是:若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象.
(2)乙同学的猜想也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试剂变红.
【实验设计】
(3)为证实丙同学的猜想,还需作如下实验,请完成如表:
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | ①排出水中溶解的氧气. |
| 2.在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油. | ②隔绝空气. |
| 实验方法 | 观察到的现象和结论 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各滴加2滴酚酞试液. | 质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明 ①过浓的氢氧化钠也会使酚酞褪色(或酚酞溶液红色是否褪去,与NaOH溶液的质量分数有关). |
| 方案二:②将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释. | ③溶液变红,说明与氢氧化钠溶液质量分数大小有关. |
5.某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请同学们一起参与此次探究之旅.
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小亮、小丽、小林三位同学设计了如下方案进行探究:
【方案评价】请判断以上设计的三个方案中,小丽同学的方案是正确的.
【方案反思】请分析另外两个方案错误的原因:反应后的溶液如果呈酸性,酚酞也不变色;因为中和反应的产物NaCl和硝酸银溶液反应也会产生白色沉淀.
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl、NaOH(填化学式)
小丽认为小亮的猜想是错误的,她的理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
【方案设计】小亮、小丽、小林三位同学设计了如下方案进行探究:
| 方案设计者 | 方案步骤 | 方案预估现象 | 方案预估结论 |
| 小亮 | 取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡 | 酚酞试液 不变色 | 恰好完全中和 |
| 小丽 | 用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸呈现的颜色与标准比色卡对照 | pH=7 | 恰好完全中和 |
| 小林 | 取少量反应后的溶液于一支试管中,并向试管中滴加稀硝酸和硝酸银溶液 | 有白色沉淀生产 | 盐酸过量,没 有完全中和 |
【方案反思】请分析另外两个方案错误的原因:反应后的溶液如果呈酸性,酚酞也不变色;因为中和反应的产物NaCl和硝酸银溶液反应也会产生白色沉淀.
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】小亮猜想:溶质有NaCl、HCl、NaOH
小丽猜想:溶质只有NaCl
小林猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl、NaOH(填化学式)
小丽认为小亮的猜想是错误的,她的理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | ③ | 小林猜想正确 |
| ④ | 有蓝色沉淀生成 | 你的猜想正确 |
6.要解决“温室效应”问题,在生活中我们可以采取的措施正确的是( )
①禁止使用化石燃料
②大力植树种草,严禁乱砍滥伐
③逐步普及太阳能等清洁能源
④大力推广乙醇汽油.
①禁止使用化石燃料
②大力植树种草,严禁乱砍滥伐
③逐步普及太阳能等清洁能源
④大力推广乙醇汽油.
| A. | ①③ | B. | ②③ | C. | ②③④ | D. | ①②③④ |
7.某元素的微粒结构示意图: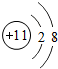 ,下列说法中,错误的是( )
,下列说法中,错误的是( )
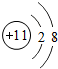 ,下列说法中,错误的是( )
,下列说法中,错误的是( )| A. | 该元素属于金属元素 | B. | 该原子的核外只有2个电子层 | ||
| C. | 该微粒属于阳离子 | D. | 该微粒具有相对稳定结构 |
8.下列过程中发生了化学变化的是( )
| A. | 湿衣服晾干 | B. | 铁水铸造成锅 | C. | 冰雪融化 | D. | 粮食酿成酒 |