题目内容
在Cu(NO3)2、A1(NO3)3和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀硫酸时有气泡产生.则反应后所得溶液中含有的金属离子有 ;反应后溶液的质量比原混合溶液的质量 (填“大”或“小”);有关反应的化学方程式为 (写出一个即可).
| 金属活动性顺序及其应用;书写化学方程式、文字表达式、电离方程式.. | |
| 专题: | 压轴实验题;金属与金属材料. |
| 分析: | 依据活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来,所以铁可以置换出铜与银但不能置换出铝,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,此现象说明Fe过量没有反应完,所以原混合溶液中的Cu(NO3)2、AgNO3全部被置换生成Cu、Ag和Fe(NO3)2溶液,A1(NO3)3不反应,再利用反应时金属的原子量可对溶液质量的改变进行分析,确定溶液质量的变化. |
| 解答: | 解:混合溶液中的Cu(NO3)2、AgNO3与铁发生置换反应,得到Cu、Ag,铁粉过量,所以滤出固体中含Fe;反应后的溶液中即滤液不再含的Cu(NO3)2、AgNO3,而是含有生成的Fe(NO3)2;由于Al(NO3)3不与Fe发生反应,所以滤液中还含有Al(NO3)3; 依据该置换反应的过程是Fe十2AgNO3=Fe(NO3) 2+2Ag;Fe+Cu(NO3) 2=Fe(NO3) 2+Cu反应的铁与铜银的原子量关系可知:该两个反应发生时铁置换银与铜时反应的铁都小于生成的铜和银,故溶液质量减小;该过程中共发现两个反应:铁和硝酸铜的置换反应,铁和硝酸银的置换反应; 故答:Al3+ 和Fe2+;小;Fe+Cu(NO3)2=Fe(NO3)2+Cu(或Fe+2AgNO3=Fe(NO3)2+2Ag). |
| 点评: | 此题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的意义,只有这样才能做出正确的判断. |

 名校课堂系列答案
名校课堂系列答案实验室常用如图所示装置探究可燃物的燃烧条件.下列说法错误的是( )
|
| A. | 烧杯中的热水只起到加热作用 |
|
| B. | 水中的白磷不能燃烧,是因为白磷没有与空气接触 |
|
| C. | 对准烧杯中的白磷通入氧气,热水中的白磷能燃烧 |
|
| D. | 铜片上的红磷不能燃烧,是因为温度没有达到着火点 |
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
(1)①此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可 能是 O2 | . | . |
| 产生此气体的一个化学方程式是 . |
②我想制取该气体,发生装置将选取下图中的 (填序号,以下同),收集装置选取 .
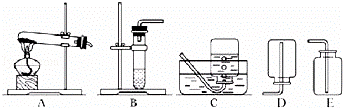
(2)我猜想无色气体还可能是另外一种气体,产生它的其中一个化学方程式是: .
(3)晴晴同学为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体2.2g.试计算:该石灰石样品中碳酸钙的质量分数.
有甲、乙、丙、丁四种金属.只有甲在自然界主要以单质形式存在.丁盐的水溶液不能用乙制的容器盛放,但可用丙制的容器盛放.这四种金属的活动性由强到弱的顺序是( )
|
| A. | 甲>乙>丁>丙 | B. | 丙>丁>乙>甲 | C. | 丙>乙>丁>甲 | D. | 乙>丁>丙>甲 |
