题目内容
我国北方某盐湖生产的纯碱产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.产生气体的质量与滴入稀盐酸的质量关系如下图所示(假设产生的气体全部逸出),当盐酸滴加至图A点时,烧杯内溶液的总质量为40.3g,.试计算:(1)A点产生气体的质量m=______.
(2)B点时,烧杯内溶液中的溶质是______(写出化学式).
(3)试样中碳酸钠的质量分数(结果精确至0.1%).
(4)所用盐酸的溶质质量分数.

【答案】分析:根据图中信息判断生成二氧化碳的质量,根据化学方程式可以计算碳酸钠的质量分数以及所用盐酸的溶质质量分数.其中加入36.5克稀盐酸时,反应已经结束.再加入稀盐酸时,反应不再进行.
解答:解:(1)A点产生气体的质量为:6g+36.5g-40.3g=2.2g.故填:2.2g;
(2)B点时反应结束,这时的溶质是氯化钠,再加入稀盐酸时溶质又多了氯化氢,这时的溶液中溶质含有氯化钠和氯化氢,故填:NaCl、HCl;
(3)设纯碱试样中碳酸钠的质量为x,36.5g稀盐酸中溶质质量为y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
x y 2.2g
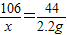
x=5.3g
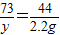
y=3.65g
试样中碳酸钠的质量分数为: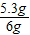 ×100%≈88.3%
×100%≈88.3%
(4)所用盐酸的溶质质量分数=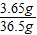 ×100%=10%
×100%=10%
答:(3)碳酸钠的质量分数为88.3%;(4)所用盐酸的溶质质量分数10%.
点评:本题主要考查了视图问题和根据化学方程式进行相关方面计算的内容.
解答:解:(1)A点产生气体的质量为:6g+36.5g-40.3g=2.2g.故填:2.2g;
(2)B点时反应结束,这时的溶质是氯化钠,再加入稀盐酸时溶质又多了氯化氢,这时的溶液中溶质含有氯化钠和氯化氢,故填:NaCl、HCl;
(3)设纯碱试样中碳酸钠的质量为x,36.5g稀盐酸中溶质质量为y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
x y 2.2g
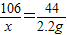
x=5.3g
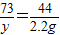
y=3.65g
试样中碳酸钠的质量分数为:
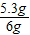 ×100%≈88.3%
×100%≈88.3%(4)所用盐酸的溶质质量分数=
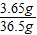 ×100%=10%
×100%=10%答:(3)碳酸钠的质量分数为88.3%;(4)所用盐酸的溶质质量分数10%.
点评:本题主要考查了视图问题和根据化学方程式进行相关方面计算的内容.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g,(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示.试计算:
我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g,(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如下图所示.试计算: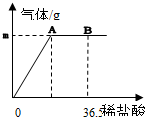 我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g,(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试计算:
我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g,(假设产生的气体全部逸出),产生气体的质量与滴入稀盐酸的质量关系如图所示.试计算: 我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算:
我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸,当盐酸滴加至36.5g时,烧杯内溶液的总质量为40.3g(假设产生的气体全部逸出).产生气体的质量与滴入稀盐酸的质量关系如图所示,试计算: (2011?保康县模拟)我国北方某盐湖生产的纯碱产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.产生气体的质量与滴入稀盐酸的质量关系如下图所示(假设产生的气体全部逸出),当盐酸滴加至图A点时,烧杯内溶液的总质量为40.3g,.试计算:
(2011?保康县模拟)我国北方某盐湖生产的纯碱产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样放在烧杯中并滴入稀盐酸.产生气体的质量与滴入稀盐酸的质量关系如下图所示(假设产生的气体全部逸出),当盐酸滴加至图A点时,烧杯内溶液的总质量为40.3g,.试计算: (2013?奉贤区二模)我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样配成溶液,向其中逐滴加入CaCl2溶液,产生沉淀物质的量与所加CaCl2的物质量关系如图所示.
(2013?奉贤区二模)我国北方某盐湖生产的纯碱(Na2CO3)产品中常含有少量的氯化钠(其它杂质忽略不计).为测定该产品中碳酸钠的质量分数,现称取6g试样配成溶液,向其中逐滴加入CaCl2溶液,产生沉淀物质的量与所加CaCl2的物质量关系如图所示.