题目内容
三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水)。
(1)小敏的方法可用如下流程表示,测得的碳酸钙质量分数为_____________;他在过滤操作中,需要用到的玻璃仪器有_______________(选填序号)。
A.酒精灯、漏斗、玻璃棒 B.漏斗、玻璃棒、烧杯 C.酒精灯、试管、玻璃棒
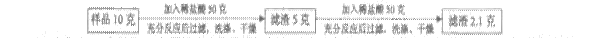
(2)小华取10克样品,用如图甲实验装置进行实验,反应结束后,测得B装置质量增加了4.6克,算得碳酸钙的质量分数,发现与事实严重不符,造成这种情况的可能原因是________________________________________________________。
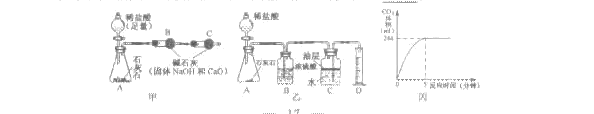
(3)小军用如图乙的实验装置进行实验,将20克稀盐酸加入到1.25克样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8克/升。求该石灰石样品中CaCO3的质量分数。
(4)求实验所用的稀盐酸的溶质质量分数。
答案:(1)79% B
(2)B中吸收了二氧化碳带出的水蒸气或HCl气体
(3)生成CO2的m=ρV=1.8克/升×0.244升≈0.44克
设参加反应的碳酸钙的质量为x,则
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
x 0.44克
1000:44=x:0.44克
x=1克
CaCO3%=1克/1.25克=80%
(4)设参加反应的稀盐酸的质量分数为y,则
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 73
5克 50克y
100:73=5克:50克y
y=7.3%
解析:(1)根据题干中“杂质既不与酸反应,也不溶于水”及流程中样品质量(10克)和最后剩余残渣质量(2.1克)可知,10克样品中含有CaCO3的质量为7.9克,及碳酸钙的质量分数为79%。过滤用到的玻璃仪器有烧杯、漏斗、玻璃棒,选B。
(2)假设10克样品中只含有CaCO3一种成分,则最多可产生CO2的质量为4.4克,实验测得装置增重4.6克,显然增重的质量不全是CO2,分析装置及药品可知,石灰石与稀盐酸反应产生CO2的同时,部分HCl会挥发逸出,同时制得的CO2中还会含有少量的水蒸气,无论HCl还是水蒸气,都能被碱石灰干燥剂吸收,因此会造成实验结果与实际严重不符的情况。
(3)解本题需用到如下计算:密度计算、化学方程式计算及质量分数计算。据图可知产生CO2的体积,结合其密度可求出产生CO2的质量,再将CO2质量带入化学方程式进行计算,可求出样品中碳酸钙的质量,将求出的碳酸钙质量与样品质量相除即可得出碳酸钙的质量分数。
(4)要求所用稀盐酸的质量分数,需用到(1)题小敏第一次加入稀盐酸的实验数据,即50克稀盐酸恰好与5克碳酸钙反应。据此根据化学方程式可求出50克稀盐酸中溶质的质量,继而根据溶质质量分数计算公式求出答案。

2011年5月1日起“醉驾入刑”。醉酒的原因是酒中含有一种物质叫乙醇,对人的神经系统有刺激作用。醉酒后驾车会带来严重的社会危害。
(1)乙醇(C2H5OH)易燃烧,燃烧的化学方程式为:______________________________。
(2)交警进行呼气酒精检测的原理是橙红色的K2Cr2O7酸性溶液遇乙醇迅速生成蓝绿色的硫酸铬,硫酸铬由Cr3+和SO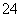 组成,则硫酸铬的化学式为____________。
组成,则硫酸铬的化学式为____________。
(3)白酒是乙醇的水溶液,酒中乙醇在微生物的作用下能被氧化成乙酸,现有一瓶密封放置了十几年的某种白酒,某兴趣小组想知道该白酒的组成情况,设计了如下探究实验:
【提出问题】白酒中溶质有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性。
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性。
【猜 想】
猜想1:只有乙醇;猜想2:只有乙酸;猜想3:______________________。
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | ①_____________________________ | 猜想3 成立 |
| ②____________________________________________________________ | ②____________________________________________________________ |
小英同学为了侧定某地区石灰石样品中碳酸钙的质量分数,取该样品15g,现将75m1的稀盐酸分三次加人石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表:
| 实验 | 第一次 | 第二次 | 第三次 |
| 加人稀盐酸的量/ml | 25 | 25 | 25 |
| 生成气体的质量/g | 2.2 | m | 1.1 |
试求:
(1)m的值是 g。
(2)求该样品中碳酸钙的质量分数(保留一位小数)?
 量为51.0g
量为51.0g ”或“偏小”或“无影响”),原因是 。
”或“偏小”或“无影响”),原因是 。 确到0.1%)
确到0.1%)