题目内容
2. 金属在生产和科学研究中有广泛的应用,请回答下列问题:
金属在生产和科学研究中有广泛的应用,请回答下列问题:(1)铝可制成铝箔是利用了它的延展性.
(2)某钢铁厂利用磁铁矿炼铁.写出该反应的化学方程式:4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
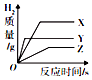
(3)把等质量、形状相同的X、Y、Z三种较活泼金属投入到足量的同种稀硫酸中,生成H2的质量与反应时间的关系如图所示.这三种金属的活动性最强的是Y.若X、Y、Z都是+2价金属,则相对原子质量最小的是X.
分析 (1)根据金属的性质决定了金属的用途进行分析;
(2)根据一氧化碳和四氧化三铁在高温的条件下生成铁和二氧化碳进行分析;
(3)根据金属的活动性越强,等质量的金属与酸反应的速率越快,化合价相同的金属,金属的相对原子质量与生成的氢气质量成反比进行分析.
解答 解:(1)铝可制成铝箔是利用了它的延展性;
(2)一氧化碳和四氧化三铁在高温的条件下生成铁和二氧化碳,化学方程式为:4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(3)通过分析三种金属的反应图象可知,Y图象的斜率最大,所以三种金属的活动性最强的是Y,X、Y、Z都是+2价金属,X金属生成的氢气最大,所以相对原子质量最小的是X.
故答案为:(1)延展;
(2)4CO+Fe3O4$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;
(3)Y,X.
点评 本题主要考查了金属的化学性质和金属活动性顺序的应用,难度不大,需要在平时的学习中加强记忆即可完成.

练习册系列答案
相关题目
12.下列图象能正确反应对应关系的是( )
| A. |  表示向等质量、等质量分数的两份稀硫酸中分别加入足量氧化镁、氢氧化镁固体 | |
| B. |  加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) | |
| C. | 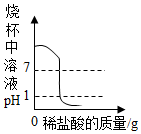 向一定质量的氢氧化钠溶液的烧杯中逐滴加入pH=1的稀盐酸至过量 | |
| D. | 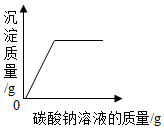 盐酸与氯化钡的混合溶液中逐滴滴入碳酸钠溶液至过量 |
13.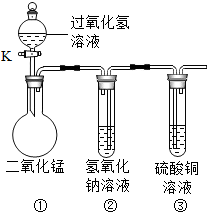 在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正 确的是( )
在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正 确的是( )
 在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正 确的是( )
在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正 确的是( )| A. | 打开活塞K,装置①中会有气泡冒出,黑色固体消失 | |
| B. | 打开活塞K,装置①中会有气泡冒出,②中液面升高 | |
| C. | 打开活塞K,装置②中看到液体流入,产生蓝色沉淀 | |
| D. | 打开活塞K,装置③中会看到液体流入,产生蓝色沉淀 |
10.下列实验操作正确的是( )
| A. | 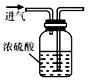 干燥氧气 | B. | 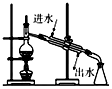 制取蒸馏水 | ||
| C. |  称量固体药品 | D. | 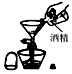 给酒精灯添加酒精 |
17.下列有关水的说法正确的是( )
| A. | 淡水资源取之不尽,无须节约 | |
| B. | 生活中可用煮沸的方法降低水的硬度 | |
| C. | 电解水的实验说明水是由氢气和氧气组成的 | |
| D. | 水可以溶解所有物质 |
7.某合金6g与足量的酸充分反应后,如果生成0.2g氢气,该合金中的元素可能是( )
| A. | Zn和Fe | B. | Cu和Au | C. | Zn和Cu | D. | Mg和A1 |
11.氮气变为液氮是因为( )
| A. | 分子的大小发生了变化 | B. | 分子间隔发生了变化 | ||
| C. | 分子停止了运动 | D. | 分子的质量发生了变化 |
12.分类是化学研究常用的方法,下列说法不正确的是( )
| A. | 氧化物:干冰、五氧化二磷、冰水共存物 | |
| B. | 金属材料:生铁、金、青铜 | |
| C. | 复合肥:磷酸钾、硝酸钾、磷酸氢二铵 | |
| D. | 天然有机高分子材料:羊毛、棉花、塑料 |