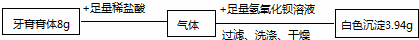题目内容
某碳酸钠样品含有少量的硫酸钠,取一定质量的该样品,完全溶解在水中配 制成100 g溶液,将其全部加入到100 g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是195.6 g,将溶液蒸干,得到15.6 g硫酸钠。 计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)原碳酸钠样品中碳酸钠的质量分数(计算结果精确到0.1%)。
解:生成二氧化碳的质量:100 g+100 g一195.6 g = 4.4 g
设样品中碳酸钠的质量为x,反应的硫酸质量为y,生成硫酸钠的质量为z。
Na2CO3+H2SO4 = Na2SO4+H2O+CO2↑
106 98 142 44
x y z 4.4 g
106:44=x:4.4 g x=10.6 g
98:44=y:4.4 g y=9.8 g
142:44=z:4.4g z=14.2g
硫酸溶液中溶质的质量分数: 9.8g/100g×100%=9.8%
原样品的质量:15.6g-14.2g+10.6g=12g
原样品中碳酸钠的质量分数:10.6/12g×100%=88.3%
答:硫酸溶液中溶质的质量分数为9.8%,原样品中碳酸钠的质量分数为88.3%

下表各选项中,实验操作一定能够达到相对应的实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 验证氧气能支持燃烧 | 把带火星的木条伸到盛有氧气的集气瓶中 |
| B | 验证二氧化碳与水反应生成碳酸 | 向收集满二氧化碳的集气瓶中加入约1/3体积的滴有酚酞的水,振荡 |
| C | 探究稀硫酸与氢氧化钠溶液恰好完全反应 | 向稀硫酸与氢氧化钠溶液反应后所得的溶液中滴加硝酸钡溶液 |
| D | 探究人体吸入的空气与呼出的气体中二氧化碳含量的不同 | 常温下,同时分别向同体积的盛有空气样品和呼出气体样品的集气瓶中滴加相同滴数的饱和澄清石灰水,振荡 |
 (3)我国是世界产煤大国。但含硫煤燃烧排放的二氧化硫,会引起“酸雨”。为减少大气污染,某发电厂采用了“石灰固硫法”,即在一定条件下向煤中掺入生石灰,用来吸收二氧化硫,已知这一过程中,各元素的化合价均未发生改变,写出“石灰固硫法”的化学方程式 。
(3)我国是世界产煤大国。但含硫煤燃烧排放的二氧化硫,会引起“酸雨”。为减少大气污染,某发电厂采用了“石灰固硫法”,即在一定条件下向煤中掺入生石灰,用来吸收二氧化硫,已知这一过程中,各元素的化合价均未发生改变,写出“石灰固硫法”的化学方程式 。

 步骤】
步骤】