题目内容
14.某碳酸钠样品中含有少量的氯化钠.课外探究小组的同学欲测定样品中碳酸钠的含量,他们取该碳酸钠样品11.0g,加入稀盐酸100.0g,样品中的碳酸钠与稀盐酸恰好完全反应,同时剩余质量105.6g试计算:(1)生成气体的质量5.4克
(2)碳酸钠样品中碳酸钠的质量.
分析 (1)根据反应前后的质量差可以计算生成二氧化碳的质量;
(2)根据二氧化碳的质量可以计算碳酸钠的质量;
解答 解:(1)由题意知生成二氧化碳的质量为:11g+100.0g-105.6g═5.4g,故填5.4;
(2)设纯碱样品中碳酸钠的质量为x,
Na2CO3+2HCl=2NaCl+CO2↑+H2O,
106 44
x 4.4g
$\frac{106}{x}=\frac{44}{5.4g}$,
x=13g,
纯碱样品中碳酸钠的质量为13g,
答:纯碱样品中碳酸钠的质量为13g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
14.火山喷发出的物质往往会造成严重的环境污染.下列物质中不属于空气污染物的是( )
| A. | 二氧化硫 | B. | 二氧化碳 | C. | 火山灰 | D. | 一氧化碳 |
6.化学是一门以实验为基础的科学.下列有关实验现象的描述中正确的是( )
| A. | 铁在氧气中燃烧,火星四射,生成四氧化三铁 | |
| B. | 硫在空气中燃烧发出蓝紫色火焰,生成二氧化硫 | |
| C. | 酚醛塑料(俗称电木)受热后熔化 | |
| D. | 镁条中加入稀盐酸有大量气泡产生,试管外壁发烫 |
4.除去下列各组物质中的杂质,所用试剂和方法中不正确的是( )
| 物质 | 杂质 | 除杂所用的试剂和方法 | |
| A | O2 | HCl气体 | 先通过NaOH,再通过浓硫酸 |
| B | NaOH溶液 | Ca(OH)2溶液 | 先加入适量的 Na2CO3溶液,过滤 |
| C | NaCl溶液 | Na2CO3溶液 | 先加入适量的澄清石灰水,过滤 |
| D | Ca(OH)2 | CaO | 加入适量的水,烘干 |
| A. | A | B. | B | C. | C | D. | D |
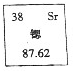 2015年中国科技令人瞩目,成果辉煌,请回答下列问题:
2015年中国科技令人瞩目,成果辉煌,请回答下列问题: