题目内容
10.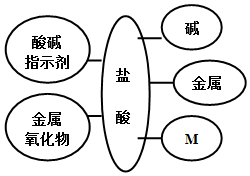 构建知识网络,可以帮助我们理解知识间的内在联系.右图是盐酸与不同类别物质之间反应的知识网络.
构建知识网络,可以帮助我们理解知识间的内在联系.右图是盐酸与不同类别物质之间反应的知识网络.(1)图中M应为盐类物质.
(2)写出用盐酸除铁锈(主要成分Fe2O3)的化学方程式是6HCl+Fe2O3=2FeCl3+3H2O.
分析 把盐酸的性质用网络框架的形式表示出来,可以更直观的让学生了解和记忆.根据盐酸的化学性质:(1)跟指示剂反应,(2)跟活泼金属起置换反应,(3)跟碱性氧化物反应,(4)跟某些盐反应,(5)跟碱起中和反应 据此结合盐酸溶液的一些典型反应即可解答本题.
解答 解:(1)盐酸可与五类物质发生化学反应,图中M应为其中的盐类物质;
(3)铁锈属于金属氧化物,与盐酸反应生成盐和水,反应中元素的化合价不变,化学方程式为:6HCl+Fe2O3=2FeCl3+3H2O;
故答案为:(1)盐;(2)6HCl+Fe2O3=2FeCl3+3H2O.
点评 盐酸是酸的代表物质,熟记酸的通性是解决此类问题的关键所在,属基础性知识考查题.

练习册系列答案
相关题目
20.以下是净水的操作,单一操作相对净化程度由低到高的排列顺序正确的是( )
①静置沉淀 ②过滤 ③吸附沉淀 ④蒸馏.
①静置沉淀 ②过滤 ③吸附沉淀 ④蒸馏.
| A. | ①②③④ | B. | ①③②④ | C. | ①④②③ | D. | ③①②④ |
18.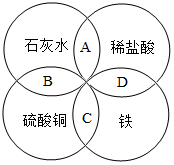 铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )
铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )
 铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )
铁、盐酸、石灰水、硫酸铜是初中化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质间反应的主要实验现象,其中描述不正确的是( )| A. | A无明显现象产生 | B. | B有红褐色沉淀 | ||
| C. | C有红色固体析出产生 | D. | D有气泡生成 |
5.甲、乙两车间排放出的污水中分别含有大量且不同的4种离子,这些离子是Ag+、Ba2+、Fe3+、Na+、Cl-、NO3-、OH-、SO42-.经检测,甲车间的污水pH>7,则下列判断正确的是( )
| A. | 甲车间的污水中可能含有Ba2+ | B. | 乙车间的污水中可能含有Na+ | ||
| C. | 乙车间的污水中一定含有Fe3+ | D. | 甲车间的污水中不可能含有SO42- |
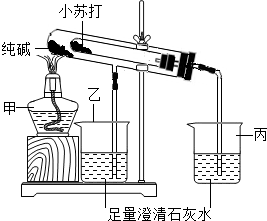 某化学兴趣小组设计了如图所示的装置,对纯碱(Na2CO3)和小苏打(NaHCO3)两种固体进行实验探究.
某化学兴趣小组设计了如图所示的装置,对纯碱(Na2CO3)和小苏打(NaHCO3)两种固体进行实验探究.