题目内容
11.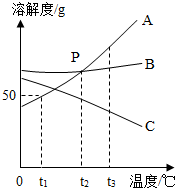 A,B,C三种固体物质的溶解度曲线如图所示,回答下列问题:
A,B,C三种固体物质的溶解度曲线如图所示,回答下列问题:(1)当A中混有少量的B,常用的提纯方法是降温结晶.
(2)将A,B,C三种物质的饱和溶液从t2℃将到t1℃,所得溶液中溶质的质量分数关系由大到小的顺序是B、A、C.
(3)说出图中P点表示的意义t2℃时,A、B物质的溶解度相等.
(4)t1℃,将50gA物质放于50g水中,充分溶解后,所得溶液的质量是75g.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)A物质的溶解度受温度影响变化较大,所以当A中混有少量的B,常用的提纯方法是降温结晶;
(2)t1℃时,B物质的溶解度最大,C物质的溶解度次之,A物质的溶解度最小,降低温度,A、B物质会析出晶体,C物质不会,C物质应该按照t2℃时的溶解度计算,所以将A,B,C三种物质的饱和溶液从t2℃将到t1℃,所得溶液中溶质的质量分数关系由大到小的顺序是B、A、C;
(3)图中P点表示的意义是:t2℃时,A、B物质的溶解度相等;
(4)t1℃,A物质的溶解度是50G,所以将50gA物质放于50g水中,充分溶解后,所得溶液的质量是75g.
故答案为:(1)降温结晶;
(2)B、A、C;
(3)t2℃时,A、B物质的溶解度相等;
(4)75.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列实验方案正确的是( )
| 选项 | 实验目的 | 方案 |
| A | 鉴别氯化铵和硝酸铵两种化肥 | 各取化肥少量,分别加入少量的熟石灰,混合、研磨,闻气味 |
| B | 从氯化钾和二氧化锰的混合物中提纯二氧化锰 | 将混合物溶于足量的水,然后过滤、洗涤、干燥 |
| C | 除去氯化钠溶液中的氯化钙 | 加入过量的碳酸钠溶液 |
| D | 检验二氧化碳气体 | 用燃烧的木条,火焰熄灭为二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
19.实验室部分装置如图所示,回答下列问题(制取时将A中的药品混合).
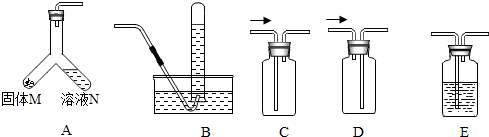
(1)制取并收集不同气体,填写如表空白.
(2)收集干燥的CO2还需要用装置E,E中盛装的试剂为浓硫酸.
(3)用上述装置A制取O2时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.

(1)制取并收集不同气体,填写如表空白.
| 固体M | 溶液N | 制取的气体 | 收集装置(填字母) |
| 大理石 | CO2 | ||
| 锌粒 | 稀硫酸 | B或D | |
| O2 | B或C |
(3)用上述装置A制取O2时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
6.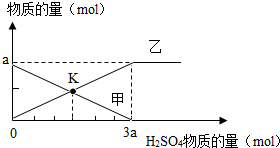 向amolFe2O3中滴加稀硫酸,随着硫酸的加入,有关量的变化见图,分析错误的是( )
向amolFe2O3中滴加稀硫酸,随着硫酸的加入,有关量的变化见图,分析错误的是( )
 向amolFe2O3中滴加稀硫酸,随着硫酸的加入,有关量的变化见图,分析错误的是( )
向amolFe2O3中滴加稀硫酸,随着硫酸的加入,有关量的变化见图,分析错误的是( )| A. | 曲线甲表示氧化铁的物质的量 | |
| B. | 曲线乙表示生成水的物质的量 | |
| C. | K点时溶液中铁元素的物质的量是amol | |
| D. | K点时硫酸铁和剩余氧化铁物质的量相等 |
16.如图为某原子的结构示意图,该原子的原子核中有( )
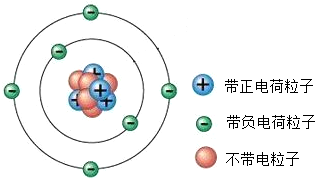

| A. | 6个质子和8个中子 | B. | 8个质子和6个中子 | ||
| C. | 6个质子和8个电子 | D. | 8个质子和6个电子 |
20.在生活中,下列过程发生了化学变化的是( )
| A. | 水果榨成果汁 | B. | 木材制家具 | C. | 粮食酿酒 | D. | 玉石雕刻印章 |
1.家庭常用的某种消毒液中的主要成分是次氯酸钠(NaClO),次氯酸钠中氯元素的化合价是( )
| A. | -1 | B. | +1 | C. | +3 | D. | +5 |
 是钠原子的结构示意图,该原子在化学反应中容易失去电子(填“得到”或“失去”).
是钠原子的结构示意图,该原子在化学反应中容易失去电子(填“得到”或“失去”).