题目内容
18.有两瓶失去标签的无色溶液,其中一瓶是NaOH溶液,另一瓶是Na2CO3溶液.(1)为鉴别两种溶液,下列选项不可行的是C.
A.稀盐酸 B.石灰水 C.氯化钠溶液
(2)小明同学想测知碳酸钠溶液中溶质的质量分数,取20克碳酸钠溶液于烧杯,再往烧杯中滴加10%的稀盐酸至没有气泡产生,共用去稀盐酸73克,则此碳酸钠溶液中溶质的质量分数是多少?
分析 (1)根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质与同种物质反应的现象相同,则无法鉴别它们.
(2)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,由参加反应的稀盐酸的质量、溶质的质量分数,由反应的化学方程式,列式计算出参加反应的碳酸钠的质量,进而计算出此碳酸钠溶液中溶质的质量分数即可.
解答 解:(1)A、稀盐酸能与碳酸钠溶液反应生成氯化钠、水和二氧化碳气体,与氢氧化钠发生中和反应生成氯化钠和水,但无明显变化;分别滴加稀盐酸,产生气泡的是碳酸钠溶液,无明显变化的是氢氧化钠溶液,可以鉴别,故选项正确.
B、石灰水能与碳酸钠溶液反应生成碳酸钙白色沉淀和氢氧化钠,与氢氧化钠不反应,但无明显变化;分别滴加石灰水,产生白色沉淀的是碳酸钠溶液,无明显变化的是氢氧化钠溶液,可以鉴别,故选项正确.
C、氯化钠溶液与NaOH溶液、Na2CO3溶液均不反应,不能出现两种明显不同的现象,不能鉴别,故选项错误.
(2)10%的稀盐酸73克中含溶质的质量为73g×10%=7.3g.
设参加反应的碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73
x 7.3g
$\frac{106}{73}=\frac{x}{7.3g}$ x=10.6g
此碳酸钠溶液中溶质的质量分数是$\frac{10.6g}{20g}$×100%=53%.
答:(1)C;(2)此碳酸钠溶液中溶质的质量分数是53%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算、物质的鉴别方法是正确解答本题的关键.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
8.下列实验操作或装置正确的是( )
| A. |  点燃酒精灯 | B. |  实验室制取氧气 | ||
| C. |  检验气密性 | D. |  过滤 |
9.武德合金用作保险丝的原因是( )
| A. | 熔点低 | B. | 硬度低 | C. | 较美观 | D. | 成本低 |
6.下列变化中,属于化学变化的是( )
| A. | 蜡烛熔化 | B. | 钢铁生锈 | C. | 工业制氧气 | D. | 车胎爆炸 |
10.56g镁、铁、锌的混合物跟足量稀硫酸反应后得到的混合溶液,经蒸发后得到200g无水硫酸盐,则反应产生的氢气的质量是( )
| A. | 2g | B. | 3g | C. | 3.5g | D. | 4.5g |
5.下列说法中不正确的是( )
| A. | 分子、原子、离子都可以构成物质 | B. | 原子是化学反应中的最小粒子 | ||
| C. | 同种元素组成的物质一定是单质 | D. | “热胀冷缩”现象表明分子间有间隔 |
6. 寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.
寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.
【猜想】
甲同学猜想:硫燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:硫燃烧后瓶内的二氧化硫(不支持硫的燃烧)浓度过高导致硫熄灭了;
丙同学猜想:甲和乙都只看到了问题的一个方面,他认为甲和乙都有道理;
丁同学猜想:硫燃烧消耗氧气导致氧气浓度太低而熄灭.
【设计实验】丁同学设计了实验2进行实验验证自己的猜想:
【实验反思】(1)硫燃烧的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;实验2中硫燃烧的火焰颜色是淡蓝色.
(2)实验1与课本实验相比,实验1的优点是避免SO2对大气污染;
(3)实验2中细沙的作用是防止红磷燃烧放出的热量使集气瓶炸裂.
(4)实验室中测定空气中氧气体积分数实验不用硫代替红磷的原因是硫燃烧生成气体使气压变化不明显.
 寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.
寿春中学化学组的同学设计了硫在氧气中燃烧的改良实验,如实验1.当火焰熄灭后发现留有剩余,硫为什么会熄灭呢?每个人都提出了自己的猜想.【猜想】
甲同学猜想:硫燃烧耗尽了瓶内的氧气,所以它熄灭了;
乙同学猜想:硫燃烧后瓶内的二氧化硫(不支持硫的燃烧)浓度过高导致硫熄灭了;
丙同学猜想:甲和乙都只看到了问题的一个方面,他认为甲和乙都有道理;
丁同学猜想:硫燃烧消耗氧气导致氧气浓度太低而熄灭.
【设计实验】丁同学设计了实验2进行实验验证自己的猜想:
| 实验步骤 | 实验现象 | 实验分析 | 实验结论 |
| (1)把少量红磷放在铝制小盒内,然后放入装有细沙的集气瓶,塞紧瓶塞,用放大镜点燃硫,观察现象. | 硫燃烧一会儿就熄灭了. | 磷燃烧需满足的条件:①温度达到着火点; ②与氧气接触 | 丁同学的猜想正确. |
| (2)待冷却后,用放大镜聚光加热铝盒内的红磷,观察现象. | 红磷燃烧,放出热量的同时产生了白烟 |
(2)实验1与课本实验相比,实验1的优点是避免SO2对大气污染;
(3)实验2中细沙的作用是防止红磷燃烧放出的热量使集气瓶炸裂.
(4)实验室中测定空气中氧气体积分数实验不用硫代替红磷的原因是硫燃烧生成气体使气压变化不明显.
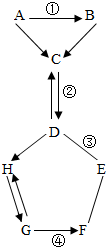 如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质,气体C常用于灭火,G是最轻的气体.请你回答:
如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质,气体C常用于灭火,G是最轻的气体.请你回答: