题目内容
5.对于化学反应:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,下列说法正确的是( )①参加反应的物质是磷和氧气 ②反应前后分子总数不变 ③反应前后元素的种类不变
④反应前后原子的种类和数目不变 ⑤反应前后物质的总质量不变 ⑥反应前后元素的化合价不变.
| A. | ①②⑥ | B. | ②③④⑤ | C. | ①②③④⑤ | D. | ①③④⑤ |
分析 化学方程式的含义有:反应物和生成物的种类;反应的条件;反应物和生成物的微观粒子个数比;反应物和生成物的质量比等.
解答 解:由化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5可知,参加反应的物质是磷和氧气,反应条件是点燃,反应前后元素的种类不变,反应前后原子的种类和数目不变,反应前后物质的总质量不变.
故选D
点评 解答本题的关键是要充分理解化学方程式的含义,只有这样才能对化学方程式表示的意义做出正确的判断.

练习册系列答案
相关题目
15.向AgNO3溶液中加入一定质量Fe和Al,充分反应后过滤,得到滤渣和浅绿色滤液.下列说法正确的是( )
| A. | 滤液中一定含有Al3+、Ag+ | B. | 滤液中一定含有Fe2+、Ag+ | ||
| C. | 滤渣中一定含有Fe | D. | 滤渣中一定含有Ag |
16.盛装浓硫酸的试剂瓶上贴有的标志是( )
| A. |  | B. |  | C. |  | D. |  |
13.厨房中报警器检测到煤气泄漏,从分子性质角度解释,这是利用( )
| A. | 分子很小 | B. | 分子在不断地运动 | ||
| C. | 分子之间有间隙 | D. | 分子可以再分 |
20.除去下列物质中的少量杂质,方法错误的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的方法 |
| A | CO | CO2 | 通过足量的氢氧化钠溶液,干燥 |
| B | Cu | Fe | 加入足量的稀硫酸,过滤,洗涤,干燥 |
| C | CaO | CaCO3 | 加入适量的稀盐酸,过滤,洗涤,干燥 |
| D | KCl溶液 | CuCl2 | 加入适量的氢氧化钾溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
10.如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图.下列说法正确的是( )
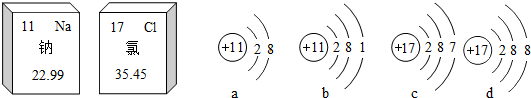
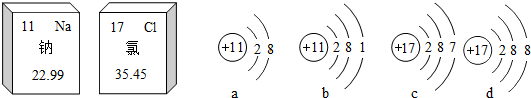
| A. | 钠、氯都属于金属元素 | B. | 氯化钠是由a、d两种粒子构成的 | ||
| C. | 氯的相对原子质量是35.45g | D. | a表示的是一种阴离子 |
17.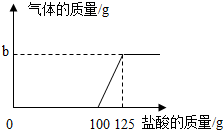 在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
(1)a的数值为125,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析)滴加盐酸至100g时,开始时有二氧化碳生成,证明有碳酸钙存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钙反应,从而证明氢氧化钙存在.
(2)b的数值为2.2.计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
 在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.
在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂.他们对该试剂进行了定量实验分析:称取试剂19.8g放入锥形瓶中,加入30.2g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如下.请根据有关信息回答问题.| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
| 锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(2)b的数值为2.2.计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
2.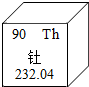 钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )
钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )
 钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )
钍将可能取代汽油成为汽车的动力来源,钍元素的相关信息如图.下列有关钍的说法正确的是( )| A. | 原子的中子数是90 | B. | 属于非金属元素 | ||
| C. | 原子核外电子数是90 | D. | 相对原子质量为232.04g |
3.下列认识正确的是( )
| A. | 聚乙烯和聚氯乙烯都可以包装食品 | |
| B. | 灼烧蛋白质时产生烧焦羽毛的气味 | |
| C. | 普通玻璃和有机玻璃都属于无机非金属材料 | |
| D. | 铁加入稀硫酸中得到黄色溶液 |