题目内容
9.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便.下列各组物质中,符合“氧化物-酸-碱-盐”顺序排列的是( )| A. | HClO HCl Mg(OH)2 MgCl2 | B. | CO2 H2CO3 CaCO3 Ca(HCO3)2 | ||
| C. | H2O HNO3 Cu(OH)2 NH4NO3 | D. | SO3 NaHSO4 NaOH Na2SO4 |
分析 氧化物是由两种元素组成并且一种元素是氧元素的化合物,电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子和酸根离子组成的化合物是盐.
解答 解:A、次氯酸和盐酸属于酸,氢氧化镁属于碱,氯化镁属于盐,故选项错误;
B、二氧化碳属于氧化物,碳酸属于酸,碳酸钙、碳酸氢钙属于盐,故选项错误;
C、水属于氧化物,硝酸属于酸,氢氧化铜属于碱,硝酸铵属于盐,故选项正确;
D、三氧化硫属于氧化物,硫酸氢钠、硫酸钠属于盐,氢氧化钠属于碱,故选项错误.
故选C.
点评 本题主要考查物质的分类,解答时要从氧化物,酸碱盐的概念方面进行分析、判断,从而得出正确的结论.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
19.能用于鉴别空气、氮气和氧气的最简便方法是( )
| A. | 带火星的木条试验 | B. | 加入澄清石灰水 | ||
| C. | 燃着的木条试验 | D. | 闻气味 |
20.戊二醛(C5H8O2)是一种预防“禽流感”的高效消毒剂.下列说法正确的是( )
| A. | 戊二醛属于氧化物 | |
| B. | 戊二醛由5个碳原子、8个氢原子、2个 氧原子构成 | |
| C. | 戊二醛中碳、氢、氧元素质量比为5:8:2 | |
| D. | 戊二醛中碳元素的质量分数最高 |
17.三草酸合铁酸钾晶体K3[Fe(C3O4)3]•3H2O可用于摄影和蓝色印刷.某研究小组将无水三草酸合铁酸钾在一定条件下加热分解后,着手探究所得含碳元素气体产物的成分.
(1)提出合理假设
假设1:只含有CO; 假设2:只含有CO2;假设3:同时含有CO和CO2.
(2)设计实验方案证明“假设3”成立(不用在答题卡上作答)
(3)实验过程:收集两瓶产生的气体,并标记为A和B. 根据(2)中方案进行实验.(所用药品和仪器任取)在答题卡上按下表的格式写出实验步骤、预期现象与结论.
(1)提出合理假设
假设1:只含有CO; 假设2:只含有CO2;假设3:同时含有CO和CO2.
(2)设计实验方案证明“假设3”成立(不用在答题卡上作答)
(3)实验过程:收集两瓶产生的气体,并标记为A和B. 根据(2)中方案进行实验.(所用药品和仪器任取)在答题卡上按下表的格式写出实验步骤、预期现象与结论.
| 实验步骤 | 预期现象与结论 |
| 步骤1:将一红亮的铜丝在酒精灯上加热变黑,然后迅速伸入A瓶中,观察. | 铜丝由黑变为红色 结论:瓶中气体含有CO |
| 步骤2: |
4.小科同学对研究物质的酸碱性产生了浓厚的兴趣,他测得家中某些物质近似的pH如表:
小科将自制的紫菜薹汁滴入上述7种物质中,发现紫菜薹汁与紫色石蕊试液的变化相似,将紫菜薹汁滴入肥皂液中,液体变成绿色.
(1)若将紫菜薹汁滴入护发素中,你认为液体的颜色变红色(填“不变”、“变红色”或“变绿色”).
(2)查阅资料:人体胃液pH在0.5-1.5之间,小科同学懂得了患胃酸过多的病人不能空腹食用上述食物中的苹果汁.
| 物质 | 洁厕灵 | 苹果汁 | 护发素 | 玉米粥 | 洗发水 | 肥皂液 | 厨房清洁剂 |
| pH | 1 | 3 | 6 | 7~8 | 8 | 10 | 12 |
(1)若将紫菜薹汁滴入护发素中,你认为液体的颜色变红色(填“不变”、“变红色”或“变绿色”).
(2)查阅资料:人体胃液pH在0.5-1.5之间,小科同学懂得了患胃酸过多的病人不能空腹食用上述食物中的苹果汁.
1.某同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂.因此,他停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行了如下探究,请你和他一起完成探究活动.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
猜想一:溶质只有氯化钙;
猜想二:可能是CaCl2和Ca(OH)2;
猜想三:含有盐酸和氯化钙.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
【方案评价】该同学与同学们通过讨论认为:
(1)方案一能证明猜想二正确,但不能证明猜想一正确.
(2)方案二可行.但该同学在记录时未记录完整,请你帮他将方案二补充完整.
【方案反思】方案一不能证明猜想一正确的理由是酚酞不变色还可能是含有盐酸和氯化钙.
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤即得只含有氯化钙的废液.
【结论】在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
猜想一:溶质只有氯化钙;
猜想二:可能是CaCl2和Ca(OH)2;
猜想三:含有盐酸和氯化钙.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 酚酞不变色 | 猜想一正确 |
| 酚酞变红色 | 猜想二正确 | ||
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入碳酸钠溶液至过量 | 先有气泡冒出,然后会有沉淀 | 猜想三正确 |
(1)方案一能证明猜想二正确,但不能证明猜想一正确.
(2)方案二可行.但该同学在记录时未记录完整,请你帮他将方案二补充完整.
【方案反思】方案一不能证明猜想一正确的理由是酚酞不变色还可能是含有盐酸和氯化钙.
【拓展与应用】实验证明猜想三是正确的.要想使溶液中的溶质只有氯化钙,你认为应该进行的实验步骤是向废液中加入碳酸钙,当不再产生气泡时,停止加入碳酸钙,过滤即得只含有氯化钙的废液.
【结论】在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量.
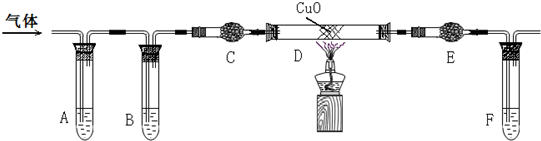
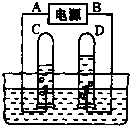 是实验室如图电解水的简易装置示意图.
是实验室如图电解水的简易装置示意图.