题目内容
14.Na2SO4是制造纸张、药品、染料稀释剂等的重要原料.某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如图1所示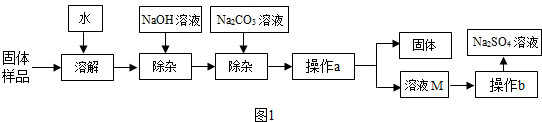
(1)加入Na2CO3溶液可除去的阳离子是Ca2+(填离子符号),其反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.若添加的NaOH溶液和Na2CO3溶液过量,可加入适量稀硫酸(填名称)除去.
(2)操作a的名称是过滤,该操作中需要用到的玻璃仪器有烧杯、玻璃棒、漏斗.
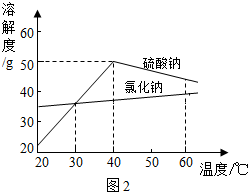
(3)溶液M中的溶质是Na2SO4和杂质NaCl,观察图2中溶解度曲线,则操作b是:先将溶液M蒸发浓缩,再降温结晶、过滤.降温结晶的最佳温度范围是30℃以下,因为Na2SO4溶解度30℃以下硫酸钠的溶解度受温度影响比氯化钠大.
分析 (1)根据本题给出的除去杂质选用的试剂,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,写出反应的化学方程式即可;如果氢氧化钠和碳酸钠过量,可加入适量的稀硫酸,稀硫酸和氢氧化钠反应生成硫酸钠和水,稀硫酸和碳酸钠反应生成硫酸钠、水和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂的原则;
(2)根据分离的物质的特征及过滤操作所需的仪器进行分析解答;
(3)根据硫酸钠和氯化钠的溶解度曲线变化分析.
解答 解:(1)加入的碳酸钠钠和氯化钙反应生成碳酸钙沉淀和氯化钠,因此除去的是钙离子,反应的化学方程式分别为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
稀硫酸和氢氧化钠反应生成硫酸钠和水,没有带入新杂质;碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳气体,没有带入任何其它杂质;符合除杂的原则,故NaOH和Na2CO3如果添加过量了,可在过滤后向滤液中滴加稀硫酸除去;
(2)操作a得到的是固体和液体,因此是过滤,过滤需要烧杯、玻璃棒、漏斗、铁架台;
(3)由于硫酸钠的溶解度在30℃以下比氯化钠小,降温的过程中会析出大量的硫酸钠,所以操作b应为:先将溶液M蒸发浓缩,再降温结晶、过滤.降温结晶的最佳温度范围是30℃以下.
故答案为:(1)Ca2+,Na2CO3+CaCl2=CaCO3↓+2NaCl;稀硫酸;
(2)过滤;漏斗;
(3)30,在30℃以下硫酸钠的溶解度比氯化钠小,且硫酸钠的溶解度受温度影响比氯化钠大.
点评 本题综合性较强,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质),掌握盐的化学性质、化学方程式的书写、过滤操作及降温结晶等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.中考复习阶段,小明同学梳理了以下知识:①太阳能、风能和天然气都是可再生能源;②洗涤剂用来洗涤油污,是因为洗涤剂能溶解油污;③生活中通过煮沸降低水的硬度;④在粗盐提纯实验中,蒸发溶液时,等到水全部蒸干才移走酒精灯;⑤合成材料包括塑料、合成纤维、合成橡胶等;⑥水是最常见的溶剂,通过初中化学所学的四种基本反应类型均可生成水;上面说法正确的是( )
| A. | ②⑤⑥ | B. | ①③⑥ | C. | ③⑤⑥ | D. | ③④⑤ |
5.下列化学用语表达正确的是( )
| A. | 氧化铁-----FeO | B. | 两个氧原子-----O2 | ||
| C. | 四个铵根离子-----4NH3+ | D. | 三个氮分子-----3N2 |
2.下列几种常见的饮料中,不含有机物的可能是( )
| A. | 果汁 | B. | 牛奶 | C. | 矿泉水 | D. | 啤酒 |
9.在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示.下列有关说法不正确的是( )
| 物质 | a | b | c | d |
| 反应前的质量/g | 30 | 20 | 10 | 15 |
| 反应后的质量/g | X | y | 0 | 10 |
| A. | 参加反应的c与d的质量比为2:1 | B. | x的取值范围:0≤x≤30 | ||
| C. | 当y≤20时,该反应一定是化合反应 | D. | x+y=65 |

 根据如图回答下列问题:
根据如图回答下列问题: