题目内容
19.农药波尔多液是由胆矾(CuSO4•5H2O)、熟石灰和水混合而成,用化学方程式表示铁制容器不能盛放波尔多液的原因是Fe+CuSO4═Cu+FeSO4.分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:铁的活动性比铜强,能把铜从硫酸铜溶液中置换出来,生成铜和硫酸亚铁,不能使用铁制容器盛放,否则会导致药效降低,反应的化学方程式为:Fe+CuSO4═Cu+FeSO4.
故答案为:Fe+CuSO4═Cu+FeSO4.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
9.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案.请你和他们一起完善下表的探究方案并回答有关问题.
(1)填表
结论:金属活动性Al>Fe>Cu
(2)将铝丝插入前应进行的操作是擦除铝丝表面的氧化铝.;
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸;
(4)小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,中需将小明同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是铜、铁、铝.
(5)通过比较、分析,可以发现上述四个反应有相似之处:均属于四种基本反应类型中的置换反应.再分析这四个反应前后各元素的化合价,我们还会发现一个相似之处:反应前后有的元素的化合价有变化.
(1)填表
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝,充分作用. | 有气泡冒出,溶液由无色变为浅绿色 |
| ②在①所得的溶液中,插入铜丝,充分作用. | 无明显现象 |
| ③在②所得的溶液中插入铝丝,充分作用. | 铝丝表面有一层黑色物质,溶液由浅绿色变无色 |
(2)将铝丝插入前应进行的操作是擦除铝丝表面的氧化铝.;
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸;
(4)小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,中需将小明同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是铜、铁、铝.
(5)通过比较、分析,可以发现上述四个反应有相似之处:均属于四种基本反应类型中的置换反应.再分析这四个反应前后各元素的化合价,我们还会发现一个相似之处:反应前后有的元素的化合价有变化.
14.下列关于元素的叙述中,正确的是( )
| A. | 同种原子的统称叫元素 | |
| B. | 同种元素的原子结构和质量完全相同 | |
| C. | 元素的种类取决于该元素原子的核外电子数 | |
| D. | 不同种元素的根本区别是核内质子数不同 |
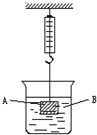 在弹簧秤下悬挂一重物A,在烧杯中盛有溶液B,根据要求回答下列问题
在弹簧秤下悬挂一重物A,在烧杯中盛有溶液B,根据要求回答下列问题