题目内容
7.某同学做粗盐(难溶性杂质)提纯实验,请根据图示回答下列问题:
(1)图④中玻璃棒的作用是搅拌,使液体受热均匀.
(2)操作⑥中的错误是缺少玻璃棒引流.
(3)粗盐提纯实验的操作顺序为①⑤②③⑥④(填操作序号)、称量精盐并计算产率.
(4)操作④中,当观察到蒸发皿中出现较多量的固体时,停止加热.
分析 (1)图④为蒸发操作,根据蒸发操作中玻璃棒的作用,进行分析解答.
(2)过滤液体时,注意“一贴、二低、三靠”的原则.
(3)粗盐的主要成分是氯化钠,盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),进行分析解答.
(4)根据蒸发操作中停止加热的时机,进行分析解答.
解答 解:(1)图④为蒸发操作,玻璃棒的作用是搅拌,使液体受热均匀.
(2)过滤液体时,要注意“一贴、二低、三靠”的原则,操作⑥中的错误是缺少玻璃棒引流.
(3)粗盐的主要成分是氯化钠,粗盐提纯实验的操作顺序为取粗盐,用托盘天平称量粗盐的质量,溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程)、称量精盐并计算产率,粗盐提纯实验的操作顺序为①⑤②③⑥④.
(4)蒸发时,待蒸发皿中出现较多量的固体时,应停止加热,利用余热将剩余液体蒸干.
故答案为:(1)搅拌,使液体受热均匀;(2)缺少玻璃棒引流;(3)①⑤②③⑥④;(4)蒸发皿中出现较多量的固体.
点评 本题难度不大,掌握粗盐提纯的原理、实验步骤(溶解、过滤、蒸发)、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
2.下列实验操作中,正确的是( )
| A. | 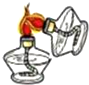 | B. |  | C. |  | D. | 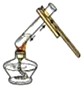 |
12.除去下列各组物质中的杂质,所选用的试剂及操作方法均正确的是(括号内的物质为杂质,所选试剂均足量)( )
| 选项 | 物质 | 选用试剂 | 操作方法 |
| A | 木炭粉(CuO) | 盐酸 | 溶解、过滤、洗涤、烘干 |
| B | CO2(CO) | NaOH溶液、浓硫酸 | 通气、加热、收集 |
| C | CaO(CaCO3) | 水 | 过滤、烘干 |
| D | NaOH(Na2CO3) | 盐酸 | 溶解、蒸发、结晶 |
| A. | A | B. | B | C. | C | D. | D |
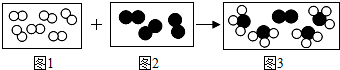
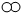 ”和“
”和“ ”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如下:
”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如下: