题目内容
14.某学校化学小组的同学,取刚降地面的雨水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如表所示:| 定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
(2)在测定的时间内,酸雨的酸性是增强(填“增强”或“减弱”)
(3)煤中含有的硫在燃烧时会以二氧化硫的形式排放,污染大气.
①硫在空气中燃烧的化学方程式是S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2.
②回收二氧化硫可以生成硫酸,化学方程式为2SO2+2H2O+O2═2H2SO4,参加反应的SO2与生成的H2SO4的质量比是32:49,将6.4t的SO2全部转化,可得到H2SO4的质量为9.8t.
分析 (1)根据表中信息分析解答;
(2)PH<5.6的雨水称为酸雨,当溶液的PH小于7时,随着PH的减小酸性增强;
(3)硫在空气中燃烧能生成二氧化硫,根据化学方程式可以进行相关方面的计算.
解答 解:
(1)根据表中信息,绘制时间-pH关系图如下: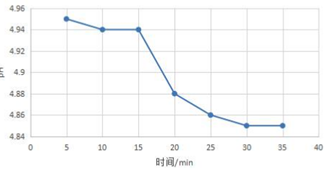
(2)在测定的时间内,雨水的PH逐渐减小,酸性逐渐增强.故填:增强.
(3)①硫在空气中燃烧的化学方程式为:S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2 .
②由2SO2+O2+2H2O=2H2SO4可知,参加反应的SO2与生成的H2SO4的质量比是:128:196=32:49.故填:32:49.
设将6.4t的SO2全部转化,可得到H2SO4的质量为x,
2SO2+O2+2H2O=2H2SO4
128 196
6.4t x
$\frac{128}{6.4t}=\frac{196}{x}$
x=9.8t.
答案:
(1)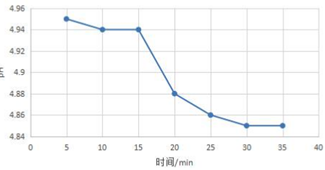
(2)增强;
(3)①S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2 .②32:49;9.8.
点评 本题考查了酸雨、化学方程式的书写、根据化学方程式计算等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
5.实验室开放日,老师给某化学兴趣小组一包氧化铜的混合物样品,要求兴趣小组测定样品中氧化铜的质量分数.同学们称取5g样品于烧杯中,再把20g稀硫酸平均分四次加入到烧杯中并进行搅拌,让其充分反应.有关实验数据记录如下:
求:
(1)氧化铜中铜元素和氧元素的质量比为4:1.
(2)硫酸分子中各原子的个数比H:S:O=2:1:4.
(3)样品中铜的质量为3g.
(4)第4次反应后所得溶液中硫酸铜的质量分数.
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入的稀硫酸的质量/g | 5 | 5 | 5 | 5 |
| 烧杯中剩余固体的质量/g | 4.2 | 3.4 | 3.0 | 3.0 |
(1)氧化铜中铜元素和氧元素的质量比为4:1.
(2)硫酸分子中各原子的个数比H:S:O=2:1:4.
(3)样品中铜的质量为3g.
(4)第4次反应后所得溶液中硫酸铜的质量分数.
2.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | NaOH | NaCl | 加入适量的稀盐酸 |
| B | FeCl2 | CuCl2 | 加入过量铁粉、充分反应后过滤 |
| C | KCl | MnO2 | 加水溶解、过滤、洗涤、干燥 |
| D | Na2SO4 | H2SO4 | 加过量的碳酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.如图表示等质量的金属Mg和Al分别与足量的相同溶质质量分数的稀硫酸反应,下列叙述正确是( )
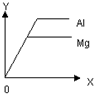

| A. | X表示滴加稀硫酸的质量,Y表示生成氢气的质量 | |
| B. | X表示生的氢气的质量,Y表示反应所用时间 | |
| C. | X表示反应时间,Y表示生成氢气的量 | |
| D. | X表示参加反应的金属的质量,Y表示生氢气的质量 |
 如图是A、B、C三种固体物质的溶解度曲线,据图回答问题:
如图是A、B、C三种固体物质的溶解度曲线,据图回答问题: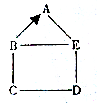 A、B、C、D、E是初中化学常见的五种不同类别的物质,其中A是导致“温室效应”的-种气体,C是一种黑色粉末.图中“--”表示相连的物质在一定条件下可以发生反应,“→”表示物质间存在转化关系.(1)物质B可能是盐酸;它的一种用途是金属除锈.(2)D与E反应的化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,其基本反应类型是复分解反应.
A、B、C、D、E是初中化学常见的五种不同类别的物质,其中A是导致“温室效应”的-种气体,C是一种黑色粉末.图中“--”表示相连的物质在一定条件下可以发生反应,“→”表示物质间存在转化关系.(1)物质B可能是盐酸;它的一种用途是金属除锈.(2)D与E反应的化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,其基本反应类型是复分解反应.