题目内容
2.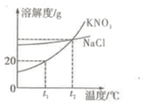 如图是KNO3和NaCl的溶解度曲线,下列说法中正确的是( )
如图是KNO3和NaCl的溶解度曲线,下列说法中正确的是( )| A. | NaCl的溶解度受温度的影响大 | |
| B. | 欲配制溶质质量分数相等的两物质的饱和溶液,所对应的温度在t1℃-t2℃之间 | |
| C. | 将含水各100g的两物质的饱和溶液,从t2℃降温至t1℃,析出晶体的质量不相等 | |
| D. | 欲从含有少量KNO3杂质的NaCl浓溶液中分离出氯化钠晶体,应降低溶液温度 |
分析 根据题目信息和溶解度曲线可知:KNO3和NaCl两种固体物质的溶解度,都是随温度升高而增大,而硝酸钾的溶解度随温度的升高变化比氯化钠大;NaCl的溶解度受温度的影响大错误;欲配制溶质质量分数相等的两物质的饱和溶液,所对应的温度在t1℃-t2℃之间错误,应该是t2℃时;将含水各100g的两物质的饱和溶液,从t2℃降温至t1℃,析出晶体的质量不相等正确;欲从含有少量KNO3杂质的NaCl浓溶液中分离出氯化钠晶体,应蒸发结晶,降低溶液温度是错误的.
解答 解:A、NaCl的溶解度受温度的影响大错误,硝酸钾的溶解度随温度的升高变化比氯化钠大;故选项错误;
B、欲配制溶质质量分数相等的两物质的饱和溶液,所对应的温度在t1℃-t2℃之间错误,应该是t2℃时,因为该温度下两种物质有交点;故选项错误;
C、将含水各100g的两物质的饱和溶液,从t2℃降温至t1℃,析出晶体的质量不相等正确,因为硝酸钾的溶解度随温度的升高变化比氯化钠大,故选项正确;
D、欲从含有少量KNO3杂质的NaCl浓溶液中分离出氯化钠晶体,应蒸发结晶,降低溶液温度是错误的,因为氯化钠的溶解度随温度的升高变化不大,故选项错误;
故选C
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液结晶的方法等,本考点主要出现在选择题和填空题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列离子能在pH=13的溶液中大量共存的是( )
| A. | Mg2+ Cl- Cu2+ NO3- | B. | H+ CO32- K+ SO42- | ||
| C. | Ba2+ Cl- NO3- Na+ | D. | NH4+ HCO3- Al3+ SO42- |
10.硬水中含有较多的可溶性钙和镁的化合物,加热时易分解为CaCO3等难溶物质而形成水垢,因此会给生活和生产带来许多影响.敏敏通过查找资料得知:大多数碳酸盐难溶于水,但雨水、河水中溶有CO2后,就会与土壤、岩石中的CaCO3、MgCO3等反应生成可溶性的碳酸氢盐进入水中,绝大多数碳酸盐都具有类似的性质.即:CaCO3+H2O+CO2═Ca(HCO3)2,Ca(HCO3)2$\frac{\underline{\;加热\;}}{\;}$CaCO3↓+H2O+CO2↑.请你结合所学知识分析,下列说法中不正确的是( )
| A. | 向澄清的石灰水中不断地通入CO2,最终一定会有白色沉淀产生 | |
| B. | 可用加热的方法除去碳酸钠固体中混有的少量碳酸氢钠 | |
| C. | 除去CO2中的HCl气体,用饱和碳酸氢钠溶液 | |
| D. | 已知相同条件下,碳酸氢钠的溶解度远小于碳酸钠的溶解度.在一定温度下,向一定量的饱和碳酸钠溶液中通入足量的CO2,有沉淀析出 |
7.下列符号中,既可以表示一个原子,又可以表示一种元素,还能表示一种物质的是( )
| A. | Cl | B. | Hg | C. | N | D. | H2 |
14.下列有关水的说法中正确是( )
| A. | 水和冰块混合得到混合物 | |
| B. | 硬水是指含有较多钙、镁化合物的水 | |
| C. | 水不仅是重要的溶剂,还能参与很多反应 | |
| D. | 电解水生成氢气和氧气,说明水是由氢原子和氧原子构成的 |
11.日常生活中发生的下列变化,属于化学变化的是( )
| A. | 瓷器破碎 | B. | 牛奶变酸 | C. | 蜡烛熔化 | D. | 酒精挥发 |
12.2014年2月11日广州署潮州市公安机关,查处12吨博大食品生产的含三聚氰胺的酸奶片.三聚氰胺的化学式C3H6N6,下列关于三聚氰胺的说法不正确的是( )
| A. | 三聚氰胺是由3个碳原子、6个氢原子、6个氮原子组成 | |
| B. | 三聚氰胺的相对分子质量为126 | |
| C. | 三聚氰胺中碳、氢、氮元素的质量比为6:1:14 | |
| D. | 三聚氰胺中氮元素质量分数为66.7% |
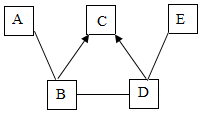 在学习了元素化合物知识后,小丽构建了以下知识网络,并对它进行了推理和判断.A~E是初中化学常见的五种不同类别的物质,E是提取量最高的金属.他们之间的关系如图所示,“-”表示相连的物质能发生反应,“→”表示一种物质能生成另一种物质(部分反应物、生成物和反应条件已略去).
在学习了元素化合物知识后,小丽构建了以下知识网络,并对它进行了推理和判断.A~E是初中化学常见的五种不同类别的物质,E是提取量最高的金属.他们之间的关系如图所示,“-”表示相连的物质能发生反应,“→”表示一种物质能生成另一种物质(部分反应物、生成物和反应条件已略去). 下列物质间的关系符号如图所示关系的是( )
下列物质间的关系符号如图所示关系的是( )