题目内容
20.请根据下列装置,回答问题: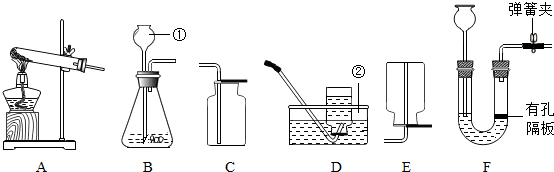
(1)写出标号①②的仪器名称:①长颈漏斗,②水槽.
(2)对于CO2、O2及H2三种气体:
①可用装置B制取的气体是CO2、O2及H2.
②可用装置C进行收集的是CO2、O2.
(3)用氯酸钾(KClO3)、二氧化锰(MnO2)及装置A制取O2
①可选用装置D(填写装置序号)能收集到较纯净的O2.
②该反应为分解反应,其化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(4)用锌粒和稀硫酸、装置F制取气体,反应过程中,用弹簧夹夹住导气管上的橡皮管,过一会儿反应就会停止.其原因是关闭弹簧夹后,U型管右端液面上方气压变大,将液体压入长颈漏斗中,固体与液体分离,反应停止.
分析 (1)根据实验室常用仪器解答;
(2)根据B用于固体与液体不加热制取气体的反应解答;根据难溶于水或不易溶于水用排水法收集,密度比空气大用向上排空气法收集,密度比空气小用向下排空气法收集解答;
(3)根据反应物的状态和反应条件确定实验室制取气体的发生装置,根据氧气的密度和溶水性确定气体的收集装置;熟记常用的化学方程式;
(4)根据装置主要是利用了气体的压强使反应随时能停止进行解答.
解答 解:
(1)根据实验室常用仪器可知:①长颈漏斗;②水槽;
(2)①B用于固体与液体不加热制取气体的反应,取二氧化碳的装置是固体和液体反应不需加热制取气体的装置,实验室用过氧化氢溶液和二氧化锰混合制取氧气不需加热,实验室用锌粒和稀盐酸混合制取氧气不需加热,故可用装置B制取的气体是CO2、O2及H2;
②C是向上排空气法收集气体,适合密度比空气大的气体,氧气的密度比空气的大,二氧化碳的密度比空气大且能溶于水,故通常用向上排空气法收集;
氢气的密度比空气的小,通常用向小排空气法收集;
(3)用KClO3与MnO2混合制取和收集纯净O2,氧气的密度比空气的大,不易溶于水,可以用用向上排空气法收集火排水法,排水法收集的角纯净,收集纯净的氧气选D;反应的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)装置F可以控制反应的进行,因为关闭弹簧夹后,U型管右端液面上方气压变大,将液体压入长颈漏斗中,固体与液体分离,反应停止.故答案为:关闭弹簧夹后,U型管右端液面上方气压变大,将液体压入长颈漏斗中,固体与液体分离,反应停止.
答案:
(1)①长颈漏斗;②水槽
(2)①CO2、O2及H2 ②CO2、O2
(3)D 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)关闭弹簧夹后,U型管右端液面上方气压变大,将液体压入长颈漏斗中,固体与液体分离,反应停止.
点评 本题考查了由装置选择制备的气体及原理、不同装置的优点以及由物质的性质选用装置,学生需要对常见气体的制备、性质熟悉,还要能够对所提供的信息进行分析运用.

| 密度(g/cm3) | 1.01 | 1.14 | 1.30 | 1.50 | 1.73 | 1.84 |
| 溶质质量分数(%) | 1 | 20 | 40 | 60 | 80 | 98 |
(2)现要将98%浓硫酸稀释到为稀硫酸,其操作为把浓硫酸缓缓地沿器壁注入盛有水的烧杯中,同时用玻璃棒不断搅拌.
(3)现有一个大烧杯,其中装有溶质质量分数为40%的硫酸,烧杯中悬浮着一个塑料小球.现往烧杯中逐滴加入一定溶质质量分数的氢氧化钡溶液,直到恰好反应为止,停止滴入氢氧化钡溶液(注:BaSO4不溶于水).
①写出上述反应的化学反应方程式:H2SO4 +Ba(OH)2=2H2O+BaSO4↓
②反应完全后,小球所处的位置是C
A.浮于液面上 B.悬浮于烧杯溶液中 C.沉于烧杯底部
你选择的理由是:当恰好完全反应时,烧杯中的液体只有水,液体密度减小.
| A. | N(NO2)3中氮元素和氧元素的原子个数是2:5 | |
| B. | N(NO2)3中氮元素和氧元素的质量比是7:4 | |
| C. | N(NO2)3相对分子质量是152g | |
| D. | N(NO2)3氮元素的质量分数是36.8% |
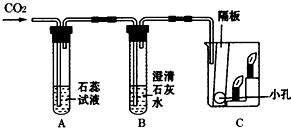 (1)小丽同学设计了右图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程为CO2+H2O=H2CO3;B中的现象是澄清石灰水变浑浊;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大;不燃烧,不支持燃烧.(答出2条即可).
(1)小丽同学设计了右图装置验证二氧化碳的性质,当通入二氧化碳一段时间后,A中发生反应的化学方程为CO2+H2O=H2CO3;B中的现象是澄清石灰水变浑浊;C中观察到蜡烛由低到高依次熄灭,说明二氧化碳的性质有二氧化碳的密度比空气大;不燃烧,不支持燃烧.(答出2条即可). 某同学设计了测定空气中氧气含量的实验,实验装置如图.
某同学设计了测定空气中氧气含量的实验,实验装置如图.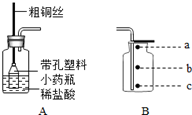 “变废为宝、爱护环境、节约资源”从我做起.宁宁家庭装修时,设计下图装置(粗铜丝可滑动)来测取二氧化碳,该反应装置通过粗铜丝调节能随时控制反应发生. 回答有关问题:
“变废为宝、爱护环境、节约资源”从我做起.宁宁家庭装修时,设计下图装置(粗铜丝可滑动)来测取二氧化碳,该反应装置通过粗铜丝调节能随时控制反应发生. 回答有关问题: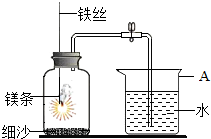 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验.在空气中点燃镁条(足量),插入密闭的集气瓶中,镁条熄灭后,待冷却至室温后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验.在空气中点燃镁条(足量),插入密闭的集气瓶中,镁条熄灭后,待冷却至室温后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%