题目内容
1.请结合如图回答问题:
(1)标号①②的仪器名称:①铁架台②长颈漏斗.
(2)实验室选用A、D装置制取O2,若加热前装置A中固体为混合物,请写出加热时装置A中发生反应的化学方程式2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,气体收集完毕时,应先从水中取出导气管(填“从水中取出导气管”或“熄灭酒精灯”),如图装置G中充满水时,也可以作为氧气的收集装置,则氧气应从b端通入(填“a”或“b”)
(3)选择发生装置B和收集装置C(选填序号)可以用于实验室制取CO2,则装置B中发生反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,若将实验室制取CO2的发生装置由B改为F,其优点是能够随时控制反应的进行或停止,某同学了解到这个优点后,他想借助于装置F用双氧水在二氧化锰的催化下制氧气,你认为该同学实验能取得成功吗?不能(填“能”或“不能”)
①为了得到纯净、干燥的CO2,除杂装置(如图2)的导管按气流方向连接顺序是c(选填字母).
a.1→2→4→3 b.2→1→3→4 c.4→3→1→2 d.3→4→2→1
用化学反应方程式表示饱和NaHCO3溶液的作用NaHCO3+HCl=NaCl+H2O+CO2↑.
②写出用澄清石灰水检验CO2的化学反应方程式CO2+Ca(OH)2═CaCO3↓+H2O.
分析 (1)熟记常见仪器的名称;
(2)如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;二氧化碳能够溶于水,密度比空气大;不同的实验装置,功能不同;
①为了得到纯净、干燥的CO2,要先除杂质再干燥;
②根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写.
解答 解:(1)①是铁架台,②是长颈漏斗;故填:铁架台;长颈漏斗;
(2)装置A适用于固体加热制取氧气,若为混合物,则为加热氯酸钾与二氧化锰的混合物,生成氯化钾和氧气;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;氧气的密度比水小,所以装置G中充满水时,收集氧气时,氧气从短管进入,水从长管排出;故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;从水中取出导气管;b;
(3)二氧化碳的密度比空气大,且能溶于水,所以用向上排空气法来收集,选择发生装置B和收集装置C可以用于实验室制取CO2,碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;若将发生装置由B改为F,其优点是能够随时控制反应的进行或停止;二氧化锰是粉末状药品,不能放在多孔隔板上,所以不能用此装置用过氧化氢在二氧化锰的催化作用下制取氧气;故填:C;CaCO3+2HCl═CaCl2+H2O+CO2↑;能够随时控制反应的进行或停止;不能;
①为了得到纯净、干燥的CO2,要先除杂质再干燥,除杂装置(如图2)的导管按气流方向连接顺序是:4→3→1→2;故填:c;
碳酸氢钠与氯化氢气体反应生成氯化钠、水和二氧化碳;故填:NaHCO3+HCl=NaCl+H2O+CO2↑;
②石灰水中的溶质是氢氧化钙,能与二氧化碳反应生成碳酸钙沉淀和水,故填:CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥、除杂和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 水能溶解所有物质 | |
| B. | 生活中常用肥皂水检验软水和硬水 | |
| C. | 长期饮用蒸馏水有利于身体健康 | |
| D. | 经过沉淀,过滤后得到的矿泉水是纯净物 |
| A. | 铜丝用作导线 | B. | 氧气用于医疗急救 | ||
| C. | 氧气用作助燃剂 | D. | 氮气用作保护气 |


 “
“ ”与“
”与“ ”的质量比是3:8(填最简整数比).
”的质量比是3:8(填最简整数比).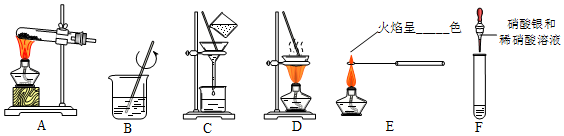

 如图是我们所熟悉的实验室制取气体的常见装置,请回答有关问题:
如图是我们所熟悉的实验室制取气体的常见装置,请回答有关问题: