题目内容
17.人类的生产和生活都离不开金属.(1)下列生活用品中,主要利用金属导热性的是C(填字母).

(2)自行车支架喷漆防锈的原理是隔绝氧气和水.
(3)我国古代湿法炼铜的反应原理是Fe+CuSO4=FeSO4+Cu(用化学方程式回答).
分析 金属具有良好的导电性、导热性和延展性;
隔绝氧气和水可以防止铁制品生锈;
我国古代湿法炼铜的反应原理是:铁和硫酸铜反应生成硫酸亚铁和铜.
解答 解:(1)利用铁制造铁锅,是利用了铁良好的导热性.
故填:C.
(2)自行车支架喷漆防锈的原理是隔绝氧气和水.
故填:隔绝氧气和水.
(3)我国古代湿法炼铜的反应原理是:铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4=FeSO4+Cu.
故填:Fe+CuSO4=FeSO4+Cu.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
7.初中化学学习了化合反应、分解反应、置换反应和复分解反应等常见的基本反应类型,而高中化学我们将重点学习氧化还原反应,有化合价升降的反应就是氧化还原反应,氧化还原反应不是基本反应类型.下列反应是氧化还原反应但不属于基本反应类型的是( )
| A. | 2KmnO4K$\frac{\underline{\;\;△\;\;}}{\;}$2MnO4+MnO2+O2↑ | B. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 2CuO+C$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ |
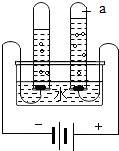
2.回答下列实验的相关问题:
(1)A中试管a中产生的气体是氧气.
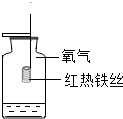
(2)B中发生反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
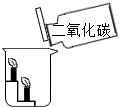
(3)C中观察到的现象是蜡烛自下而上依次熄灭.
(4)D实验得出的结论是Mg>Fe>Cu.
 |  |  | 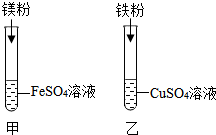 |
| A | B | C | D |
(2)B中发生反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(3)C中观察到的现象是蜡烛自下而上依次熄灭.
(4)D实验得出的结论是Mg>Fe>Cu.