题目内容
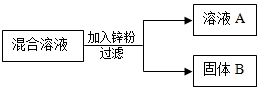 某化学小组用一定量AgNO3和Cu(NO3)2,混合溶液进行了如图实验,对溶液A和固体B的成分进行了分析和实验探究.
某化学小组用一定量AgNO3和Cu(NO3)2,混合溶液进行了如图实验,对溶液A和固体B的成分进行了分析和实验探究.[提出问题]溶液A中的溶质可能有那些?
[做出猜想]
甲同学:只有Zn(NO3)2
乙同学:Zn(NO3)2、AgNO3
丙同学:Zn(NO3)2、Cu(NO3)2
丁同学:Zn(NO3)2、AgNO3、Cu(NO3)2
[表达交流]写出丁同学猜想的理由
[反思评价]请你评价乙同学的猜想
[提出问题]固体B中的成分是什么?
[实验探究]
| 实验步骤 | 现 象 | 有关反应的化学方程式 |
| 取少量固体B,滴加 | 有气泡产生 |
考点:实验探究物质的组成成分以及含量,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:根据金属活动性顺序及其运用分析.排在氢之前的金属可与稀盐酸或稀硫酸反应产生氢气,排在前面的金属(除钾、钙、钠外)可将排在后面的金属从其盐溶液中置换出来.
解答:解:由金属活动性顺序及其运用可知,向AgNO3和Cu(NO3)2混合溶液中加入锌粉,Zn应先与AgNO3反应后与Cu(NO3)2反应.由于锌粉量的不同,溶液A中的溶质不同.当锌的量过量时,溶液中的溶质只有Zn(NO3)2;当锌的量不足恰好把溶液中的AgNO3反应完全时,溶质只有Zn(NO3)2和Cu(NO3)2;当AgNO3
有剩余时,溶液中的溶质是:Zn(NO3)2、AgNO3、Cu(NO3)2.
由以上分析可知:
[交流讨论]丁同学猜想的理由:当有AgNO3剩余时,溶质中一定含有Zn(NO3)2、AgNO3、Cu(NO3)2;
[反思评价]乙同学的猜想不合理;理由是:Zn应先与AgNO3反应后与Cu(NO3)2反应;
[实验探究]当锌粉过量时,溶液中的溶质只有Zn(NO3)2,固体B中有锌,当加入酸时有气泡生成,故下表为:
故答为:[表达交流]当有AgNO3剩余时,溶质中一定含有Zn(NO3)2、AgNO3、Cu(NO3)2;
[反思评价]不合理,Zn应先与AgNO3反应后与Cu(NO3)2反应;
[实验探究]见上表,Zn(NO3)2.
有剩余时,溶液中的溶质是:Zn(NO3)2、AgNO3、Cu(NO3)2.
由以上分析可知:
[交流讨论]丁同学猜想的理由:当有AgNO3剩余时,溶质中一定含有Zn(NO3)2、AgNO3、Cu(NO3)2;
[反思评价]乙同学的猜想不合理;理由是:Zn应先与AgNO3反应后与Cu(NO3)2反应;
[实验探究]当锌粉过量时,溶液中的溶质只有Zn(NO3)2,固体B中有锌,当加入酸时有气泡生成,故下表为:
| 实验步骤 | 现象 | 有关反应的化学方程式 |
| 稀盐酸(或稀硫酸等) | 有气泡产生 | Zn+2HCl=ZnCl2+H2↑ (或Zn+H2SO4=ZnSO4+H2↑) |
[反思评价]不合理,Zn应先与AgNO3反应后与Cu(NO3)2反应;
[实验探究]见上表,Zn(NO3)2.
点评:本题难度不是很大,主要考查了对金属活动性顺序的应用和理解,培养学生的应用能力和解决问题的能力.

练习册系列答案
相关题目
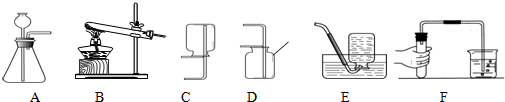
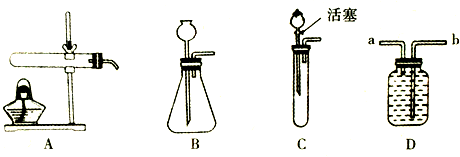
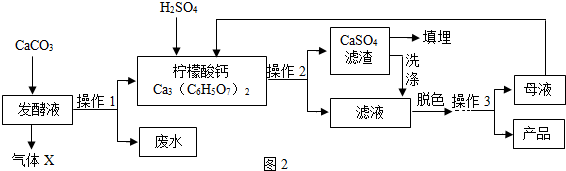
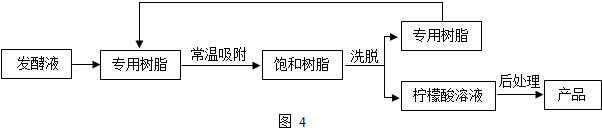
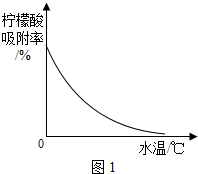 柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业,如图2、4是两种不同方法制备一水柠檬酸晶体C6H8O7?H2O)的工艺流程图,回答相关问题:
柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业,如图2、4是两种不同方法制备一水柠檬酸晶体C6H8O7?H2O)的工艺流程图,回答相关问题: