题目内容
1.据氯化钠和硝酸钾的溶解度表,回答下列问题:(溶解度单位为克)| 温度 溶解度 物质 | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 70℃ |
| NaCl | 35.8 | 36 | 36.3 | 36.6 | 37.0 | 37.3 | 37 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
(2)在50℃时,向100g水中加入90gKNO3,充分搅拌后所得溶液质量为185.5克.
(3)在10℃时,NaCl饱和溶液溶质的质量分数大于KNO3饱和溶液溶质的质量分数.(填“大于”、“等于”或“小于”)
(4)欲使硝酸钾从其常温下的饱和溶液里迅速结晶出来,应采取的办法是C
A、冷却硝酸钾的饱和溶液 B、常温下使水分蒸发
C、先加热蒸发掉一部分水,然后降温 D、升高饱和溶液的温度.
分析 (1)硝酸钾和氯化钠溶解度相同的温度即是判断该段中溶解度的数值是否存在相等的可能.
(2)根据硝酸钾在50℃时的溶解度以及溶液溶解度的相关计算知识来回答;
(3)根据饱和溶液溶质质量分数的计算方法进行计算;
(4)硝酸钾的溶解度随温度升高而增大,欲使硝酸钾从其饱和溶液中结晶出来,可采用蒸发溶剂或降低温度的方法,但欲使硝酸钾从其常温下的饱和溶液中快点结晶出来,单纯的蒸发溶剂和降温效果都不是很好,应采用加热蒸发和降温相结合的方法..
解答 解:(1)硝酸钾和氯化钠溶解度相同的温度既是判断该段中溶解度的数值是否存在相等的可能,经分析知在20~30℃时这两种物质存在溶解度相同的可能;
(2)50℃时,硝酸钾的溶解度为85.5克,向100g水中加入90gKNO3,会析出4.5克的硝酸钾,故溶液质量为100g+90g-4.5g=185.5克;
(3)在10℃时,NaCl饱和溶液溶质的质量分数=$\frac{35.8g}{100g+35.8g}$×100%=26.4%,KNO3饱和溶液溶质的质量分数=$\frac{20.9g}{100g+20.9g}$×100%=17.3%,在10℃时,NaCl饱和溶液溶质的质量分数大于KNO3饱和溶液溶质的质量分数.
(4)A、冷却常温下的硝酸钾的饱和溶液只能析出少量的硝酸钾,方法不好;
B、常温下使水蒸发,析出硝酸钾的速度会很慢,方法不好;
C、先加热蒸发掉一部分水,然后降温,可以快速的析出硝酸钾,方法最好;
D、升高温度却只能使饱和溶液变成不饱和溶液,不会析出硝酸钾晶体,方法错误.
故选C.
故答案为:(1)20℃~30℃;(2)185.5;(3)大于;(4)C.
点评 本题考查溶解度知识的具体应用,对学生深入理解溶解度的概念有一定帮助,同时也考查了饱和溶液的相关计算知识.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | 氧化铁 | B. | 黄铜 | C. | 生铁 | D. | 硬铝 |
| A. | 浓硫酸有吸水性 | |
| B. | 稀释浓硫酸时把水沿慢慢倒入浓硫酸中 | |
| C. | 浓盐酸有挥发性 | |
| D. | 浓硫酸可做某些气体的干燥剂 |
| A. | 易溶物质 | B. | 可溶物质 | C. | 微溶物质 | D. | 无法确定 |
| 实验步骤 | 实验现象 |
| ①将固体磨成粉末状,加水搅拌 | 固体没有全部溶解 |
| ②取上层清液,滴加酚酞试液 | 溶液呈红色 |
| ③取不溶物,滴加稀盐酸 | 有气泡产生 |
| A. | 一定含有Ca(OH)2,可能有CaCO3 | B. | 一定含有CaCO3和Ca(OH)2 | ||
| C. | 一定没有CaCO3和Ca(OH)2 | D. | 一定有CaCO3,可能有Ca(OH)2 |
| A. | 观察量筒里液体的体积,应该把量筒举起读数 | |
| B. | 打开试剂瓶盖应把瓶盖倒放在桌面上,标签朝着手心 | |
| C. | 滴管吸满药液后,管口要靠在试管壁上,使液体沿着试管壁流下 | |
| D. | 取放粉末状的药品要用镊子 |
| A. | 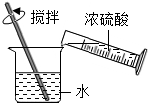 稀释浓硫酸 | B. | 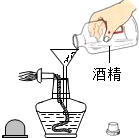 添加酒精 | ||
| C. | 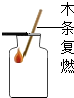 氧气验满 | D. | 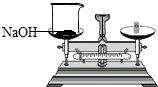 称氢氧化钠固体 |