题目内容
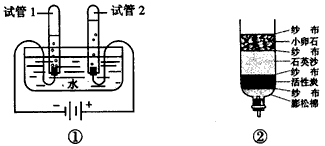
在常见的净化水的方法中,只能除去不溶性杂质的方法是
X+Cl2↑+2H2O,X的化学式为
过滤
过滤
;明矾可用于净化水,是因明矾溶于水生成胶状物可吸附
吸附
悬浮于水中的杂质;Cl2常作自来水消毒剂,其实验室制法为:MnO2+4HCl(浓)
| ||
MnCl2
MnCl2
.分析:过滤是把不溶于液体的固体与液体分离的一种方法,水的净化中明矾的作用进行分析解答.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答:解:过滤是把不溶于液体的固体与液体分离的一种方法;明矾是常用的净水剂,是利用明矾溶于水后生成的胶状物对杂质的吸附,使悬浮于水中的杂质沉降.
解:根据反应的化学方程式MnO2+4HCl(浓)
X+Cl2↑+2H2O,反应物中锰、氧、氢、氯原子个数分别为4、2、4、4,反应后的生成物中锰、氧、氢、氯原子个数分别为0、2、4、2,根据反应前后原子种类、数目不变,则每个X分子由1个锰原子和2个氯原子构成,则物质X的化学式为MnCl2.
故答案为:过滤;吸附;MnCl2.
解:根据反应的化学方程式MnO2+4HCl(浓)
| ||
故答案为:过滤;吸附;MnCl2.
点评:本题难度不大,掌握水的净化原理、化学反应前后原子守恒确定物质的化学式的方法是正确解题的关键.

练习册系列答案
相关题目


 X+Cl2↑+2H2O,X的化学式为 。
X+Cl2↑+2H2O,X的化学式为 。