题目内容
20.某化学兴趣小组选用如下图所示装置进行二氧化碳的制取和性质实验,请你根据所学知识,依图回答下列问题: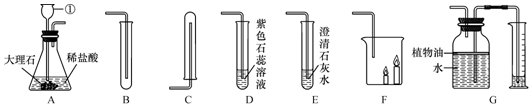
(1)请写出A中发生反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑,如用分液漏斗代替仪器①,优点是可控制反应速率.若A后面接注射器检查该装置的气密性,当加水形成液封后,缓慢拉动活塞,看到长颈漏斗下端管口产生气泡,则气密性良好.
(2)收集少量CO2气体应选择B(填装置序号),验满的方法是将燃着的木条置于试管口,若木条熄灭,证明已集满.
(3)若A与D连接,则D中出现的现象是紫色石蕊溶液变成红色,原因是CO2+H2O═H2CO3(用化学方程式表示).
(4)若A与E连接,E中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O.
(5)若A与F连接,则F中出现的现象是矮的蜡烛先熄灭,高的蜡烛后熄灭,说明了CO2具有不燃烧、也不支持燃烧的性质,因此CO2可用于灭火.
(6)G可用来测量生成CO2的体积,在水面上放一层植物油的目的是防止二氧化碳溶于水且与水反应,植物油上方原有的空气对实验的结果没有(填“有”或“没有”)明显影响.
分析 (1)根据反应的原理以及分液漏斗的特点分析.
(2)根据二氧化碳的密度比空气大解答;
(3)根据二氧化碳的性质以及酸的性质来分析;
(4)根据二氧化碳能使澄清的石灰水变浑浊来分析;
(5)根据二氧化碳灭阶梯上蜡烛的实验现象,可以判断二氧化碳的物理性质和化学性质,并且可以判断二氧化碳的用途.
(6)用碳的燃烧来制取CO2时,反应物中有气体参加,很难收集到纯净的CO2气体,或燃烧的条件下,很难将其控制在一个密闭的环境中进行,因而无法收集.
解答 解:(1)大理石的主要成分是碳酸钙,与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;将长颈漏斗换成了分液漏斗,分液漏斗可以定量控制液体的用量,其优点是可以控制反应的速率.若A后接注射器检查该装置的气密性,当加水形成液封后,缓慢拉动活塞,看到长颈漏斗下端管口产生气泡;
(2)二氧化碳的密度比空气大,所以收集少量的二氧化碳可用B装置;验满的方法是:将燃着的木条置于试管口,若木条熄灭,证明已集满;
(3)二氧化碳与水反应生成碳酸,碳酸是一种酸,能使紫色的石蕊试液变红色,该反应的化学方程式为:CO2+H2O═H2CO3;
(4)二氧化碳与澄清的石灰水反应生成碳酸钙白色沉淀和水,该反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
(5)二氧化碳的密度比空气大,不需要通过化学变化表现出来,属于二氧化碳的物理性质.二氧化碳不能燃烧,不支持燃烧,需要通过化学变化表现出来,属于二氧化碳的化学性质.若A与F连接,则F中出现的现象是矮的蜡烛先熄灭,高的蜡烛后熄灭;因为二氧化碳的密度比空气大,不能燃烧,不支持燃烧,所以二氧化碳可以用来灭火.
(6)G可用来测量生成CO2的体积,在水面上放一层植物油的目的是防止CO2溶于水且与水反应;植物油上方原有的空气对实验的结果没有明显影响.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;可控制反应速率;长颈漏斗下端管口产生气泡;(2)B;将燃着的木条置于试管口,若木条熄灭,证明已集满;(3)紫色石蕊溶液变成红色;CO2+H2O═H2CO3;(4)CO2+Ca(OH)2═CaCO3↓+H2O;(5)矮的蜡烛先熄灭,高的蜡烛后熄灭;不能燃烧;不能支持燃烧;灭火;(6)防止二氧化碳溶于水且与水反应;没有.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案| A. | 化学变化 | |
| B. | 既是化学变化又是物理变化 | |
| C. | 物理变化 | |
| D. | 可能是物理变化,也可能是化学变化 |
| A. | 蒸发5克水有晶体析出 | B. | 把温度降到0℃有晶体析出 | ||
| C. | 加入极少量的硝酸钾不溶 | D. | 以上三种方法都可以 |
| A. | ②①⑥③⑦④⑤ | B. | ②①③⑥④⑦⑤ | C. | ②⑥③①④⑦⑤ | D. | ①⑥②③④⑤⑦ |