题目内容
10.下面是四种粒子的结构示意图:
A.(1)、(2)、(3)、(4)表示3种元素,表示4种粒子;
B.表示阳离子的是(4),离子符号为Mg2+;
C.表示阴离子的是(2),离子符号为O2-;
D.表示同种元素的是(1)(2).
分析 根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的粒子是质子数相同;据此进行分析解答.
解答 解:由图示可知:
(1)质子数=核外电子数=8,为原子.
(2)质子数=8,核外电子数=10,质子数<核外电子数,为阴离子;
(3)质子数=核外电子数=10,为原子.
(4)质子数=12,核外电子数=10,质子数>核外电子数,为阳离子.
A、元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),(1)(2)的质子数相同,属于同种元素.
(1)、(2)、(3)、(4)表示3种元素,表示4种粒子;
B、(4)质子数=12,核外电子数=10,质子数>核外电子数,为阳离子.离子符号为Mg2+;
C、(2)质子数=8,核外电子数=10,质子数<核外电子数,为阴离子.离子符号为O2-;
D、元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),(1)(2)的质子数相同,属于同种元素.
故答案为:
A、3;4;
B、(4);Mg2+;
C、(2);O2-;
D、(1)(2)
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
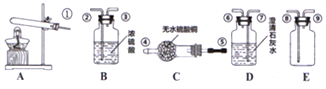
20.配制20%的NaCl溶液100g.
(1)用托盘天平称取所需的氯化钠,发现指针向右偏转,接下来的操作是A(填字母序号).
A.继续添加氯化钠 B.减少砝码
(2)用量筒量取水的体积为80 mL(ρ水≈1g/cm3).
(3)该实验的正确操作顺序为②③④①(填数字序号).
| 序号 | ① | ② | ③ | ④ |
| 操作 | 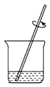 | 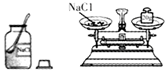 | 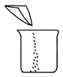 | 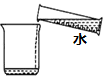 |
A.继续添加氯化钠 B.减少砝码
(2)用量筒量取水的体积为80 mL(ρ水≈1g/cm3).
(3)该实验的正确操作顺序为②③④①(填数字序号).
20.化学变化的特征是( )
| A. | 有发光发热现象 | B. | 物质的状态和颜色发生变化 | ||
| C. | 有气体放出或沉淀生成 | D. | 有其他物质生成 |
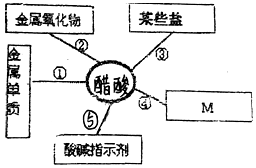 小红在学习了酸的化学性质后,在厨房发现一瓶失去标签的无色溶液,经A.闻气味;B.尝味道.初步鉴定它为白醋(主要成分为醋酸).取少量该溶液,分别倒在两个杯子里,分别加入C.纯碱(碳酸钠)、D.镁带,两个杯子均有无色气体放出,进一步证明它是醋酸.根据上述信息回答:
小红在学习了酸的化学性质后,在厨房发现一瓶失去标签的无色溶液,经A.闻气味;B.尝味道.初步鉴定它为白醋(主要成分为醋酸).取少量该溶液,分别倒在两个杯子里,分别加入C.纯碱(碳酸钠)、D.镁带,两个杯子均有无色气体放出,进一步证明它是醋酸.根据上述信息回答: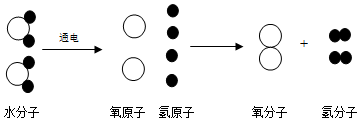
 在前两章化学学习后,我们亲身体验了分子探究实验,感受到了化学的无穷魅力.
在前两章化学学习后,我们亲身体验了分子探究实验,感受到了化学的无穷魅力.