题目内容
将25.0g大理石加入到100.0g稀盐酸中恰好完全反应,测得剩余物的质量为122.8g,求:该大理石中碳酸钙的质量分数为多少?
【答案】分析:根据质量守恒定律,放出二氧化碳的质量=反应前物质质量总和-反应后物质质量总和,而后利用碳酸钙与盐酸反应的化学方程式和生成二氧化碳的质量,列出比例式,就可计算出石灰石中碳酸钙的质量,然后根据质量分数公式计算即可.
解答:解:根据质量守恒定律,该反应放出二氧化碳的质量=25g+100g-122.8g=2.2g;
设参与反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
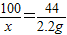 ,
,
解得:x=5g;
石灰石中碳酸钙的质量分数为: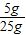 ×100%=20%.
×100%=20%.
答:该大理石中碳酸钙的质量分数为20%.
点评:本题主要考查学生利用化学方程式和质量守恒定律解答问题的能力.利用质量守恒定律,可以求出化学反应中生成气体的质量,从而为进一步解题打开突破口.
解答:解:根据质量守恒定律,该反应放出二氧化碳的质量=25g+100g-122.8g=2.2g;
设参与反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
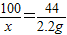 ,
,解得:x=5g;
石灰石中碳酸钙的质量分数为:
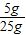 ×100%=20%.
×100%=20%.答:该大理石中碳酸钙的质量分数为20%.
点评:本题主要考查学生利用化学方程式和质量守恒定律解答问题的能力.利用质量守恒定律,可以求出化学反应中生成气体的质量,从而为进一步解题打开突破口.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
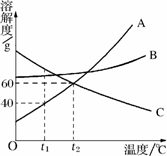
 (2012?静安区一模)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(2012?静安区一模)甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答: