题目内容
某化合物由A、B两种元素组成,其原子个数比为1:3.其中,A元素的质量分数为40%,B元素的相对原子质量为16,则A元素的相对原子质量为( )
A. 32 B. 80 C. 40 D. 16
A
解析试题分析:根据题意,某化合物由A、B两种元素组成,其原子个数比为1:3,则该化合物的化学式为:AB3;由化合物中元素的质量分数= ×100%,进行分析解答.
×100%,进行分析解答.
解:某化合物由A、B两种元素组成,其原子个数比为1:3,则该化合物的化学式为:AB3;由题意,A元素的质量分数为40%,B元素的相对原子质量为16,设A元素的相对原子质量为x,则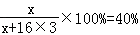 ,x=32.
,x=32.
故选A.
考点:元素的质量分数计算.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目