题目内容
9.下列物质属于混合物的是( )| A. | 水银 | B. | 生铁 | C. | 干冰 | D. | 液氮 |
分析 物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.A.水银属于纯净物中的单质,故错误.B.生铁中有铁、碳等物质,属于混合物,故正确.C.干冰属于纯净物中的氧化物,故错误.D.液氧属于纯净物中的单质,故错误
解答 解:A、水银属于纯净物中的单质,故选项错误;
B、生铁中有铁、碳等物质,属于混合物,故选项正确;
C、干冰属于纯净物中的氧化物,故选项错误;
D、液氧属于纯净物中的单质,故选项错误;
故选B
点评 本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.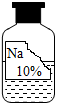 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:
【进行猜想】
猜想I:原溶液的溶质是NaCl;
猜想II:原溶液的溶质是NaOH;
猜想III:原溶液的溶质是Na2CO3;
猜想IV:原溶液的溶质是NaHCO3.
【查阅资料】
常温下,有关物质的相关信息如下表:
从物质的相关信息可知,原溶液的溶质一定不是NaHCO3,因为碳酸氢钠的饱和溶液溶质质量分数在该温度下不能达到10%.
【进行实验】
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是NaCl.
(2)同学们另取样品又进行了如下实验,实验过程如下:
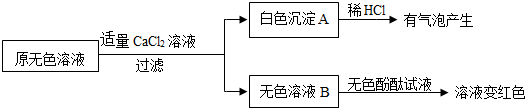
①生成白色沉淀A的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
②通过实验可以判断样品无色溶液中含有的溶质有NaOH、Na2CO3
【获得结论】
实验完成后,最终得到的结论:原瓶中的溶质是NaOH,且已变质.
 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:
实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如下图),化学小组的同学经过寻问老师后只知道是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液,为确认原瓶中是何种溶质并判断其是否变质,化学小组的同学进行了如下的探究活动:【进行猜想】
猜想I:原溶液的溶质是NaCl;
猜想II:原溶液的溶质是NaOH;
猜想III:原溶液的溶质是Na2CO3;
猜想IV:原溶液的溶质是NaHCO3.
【查阅资料】
常温下,有关物质的相关信息如下表:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下稀溶液的pH | 7 | 13 | 11 | 9 |
【进行实验】
(1)取少量样品,测得溶液的pH大于7,则原溶液的溶质肯定不是NaCl.
(2)同学们另取样品又进行了如下实验,实验过程如下:

①生成白色沉淀A的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl.
②通过实验可以判断样品无色溶液中含有的溶质有NaOH、Na2CO3
【获得结论】
实验完成后,最终得到的结论:原瓶中的溶质是NaOH,且已变质.
20.下列物质属于混合物的是( )
| A. | 干冰 | B. | 火碱 | C. | 白磷 | D. | 料酒 |
17.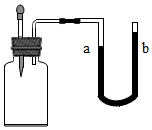 如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后,U形管内液面a低于b,不符合上述实验现象的一组试剂是( )
如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后,U形管内液面a低于b,不符合上述实验现象的一组试剂是( )
 如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后,U形管内液面a低于b,不符合上述实验现象的一组试剂是( )
如图所示:装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后,U形管内液面a低于b,不符合上述实验现象的一组试剂是( )| A. | 生石灰和水 | B. | 铁粉和稀盐酸 | C. | 硝酸铵和水 | D. | 纯碱和稀盐酸 |
1.焦亚硫酸钠在食品加工中常用作防腐剂、漂白剂和疏松剂.焦亚硫酸钠(Na2S2O5)中硫元素的化合价为( )
| A. | -2 | B. | +3 | C. | +4 | D. | +5 |
18.根据所学的化学知识,下列说法正确的是( )
| A. | SO2、NO2、CO2、CO 和可吸入颗粒物都是常见的空气污染物 | |
| B. | 电解水实验中负极产生的气体能使带火星的木条复燃 | |
| C. | 金刚石、石墨、C60化学性质相似,完全燃烧都生成CO2 | |
| D. | 用氯化钠固体配制10%的氯化钠溶液,需要用到的仪器有:天平、量筒、玻璃棒和烧杯 |
19. 根据如图所示的溶解度曲线,判断下列说法正确的是( )
根据如图所示的溶解度曲线,判断下列说法正确的是( )
 根据如图所示的溶解度曲线,判断下列说法正确的是( )
根据如图所示的溶解度曲线,判断下列说法正确的是( )| A. | 50℃时,分别将等质量的硝酸钾和氯化铵溶于适量的水恰好配成饱和溶液,所得溶液的质量前者比后者大 | |
| B. | 60℃时,把40g硝酸钾和40g氯化钾分别加入到50g水中,充分搅拌,降温至10℃,剩余晶体的质量氯化钾多 | |
| C. | 70℃时,50g硝酸钠饱和溶液与100g硝酸钾饱和溶液中所含溶剂质量之比为1:2 | |
| D. | 80℃时,向100g氯化钾饱和溶液中加入150g硝酸钠,充分搅拌后,最终得到250g溶液 |