题目内容
14.如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )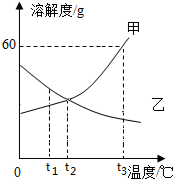
| A. | 若甲固体中含有少量乙,可采用降温结晶的方法提纯甲 | |
| B. | 将甲、乙两种物质的不饱和溶液变为饱和溶液,可以采用相同的方法 | |
| C. | 分别将等量的甲、乙的饱和溶液从t3℃降温到t2℃,所得溶液的溶质的质量分数相同 | |
| D. | 将160g溶质质量分数为20%的甲溶液稀释为10%的溶液,需要加入水的质量为60g |
分析 根据题目信息和溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;若甲固体中含有少量乙,可采用降温结晶的方法提纯甲正确,因为甲随温度升高而增大;将甲、乙两种物质的不饱和溶液变为饱和溶液,可以采用相同的方法正确,如增加溶质等;分别将等量的甲、乙的饱和溶液从t3℃降温到t2℃,所得溶液的溶质的质量分数相同错误,应该是甲的大于乙的;将160g溶质质量分数为20%的甲溶液稀释为10%的溶液,需要加入水的质量为160g,不是60g.
解答 解:A、若甲固体中含有少量乙,可采用降温结晶的方法提纯甲正确,因为甲随温度升高而增大;故选项正确;
B、将甲、乙两种物质的不饱和溶液变为饱和溶液,可以采用相同的方法正确,如增加溶质等;故选项正确;
C、分别将等量的甲、乙的饱和溶液从t3℃降温到t2℃,所得溶液的溶质的质量分数相同错误,应该是甲的大于乙的,故选项错误;
D、将160g溶质质量分数为20%的甲溶液稀释为10%的溶液,需要加入水的质量为160g,不是60g,故选项错误;
故选A、B
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了饱和溶液与不饱和溶液的转化方法等,本考点主要出现在选择题和填空题中.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
7.下列变化中属于化学变化的是( )
| A. | 大米霉变 | B. | 浓盐酸挥发 | C. | 玻璃破碎 | D. | 风力发电 |
8.物质的性质决定其用途,下列因果关系不成立的是( )
| A. | 稀有气体化学性质稳定,可用作保护气 | |
| B. | 干冰升华吸热,可用于人工降雨 | |
| C. | 熟石灰呈碱性,可用来改良酸性土壤 | |
| D. | 稀硫酸能与金属反应,可用来除锈 |
9.运送汽油的油罐车必须悬挂的标志是( )
| A. |  | B. |  | C. |  | D. |  |
19.向装有100g 水的A、B、C烧杯中分别加入25g、35g、45gKNO3固体,充分溶解后,现象如图一所示,下列说法中正确的是( )
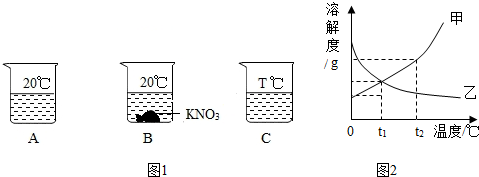

| A. | 20℃时KN03溶解度为25g | |
| B. | 烧杯B中的溶液一定属于饱和溶液 | |
| C. | 图二中能表示KNO3溶解度曲线的是乙 | |
| D. | 若将甲、乙两种物质的饱和溶液从t2℃降温至t1℃,二者仍为饱和溶液 |
6.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂,下列有关高铁酸钠的说法正确的是( )
| A. | 属于有机化合物 | B. | 由两种金属和一种非金属组成 | ||
| C. | 铁元素的质量分数为33.73% | D. | 钠、铁、氧三种元素质量比是2:1:4 |
3.关于生活中的化学,下列说法正确的是( )
| A. | 生话污水不是化工废水,可向江河湖泊里任意排放 | |
| B. | 打开易拉罐时,有大量气泡涌出是因为温度升高气体溶解度减小 | |
| C. | 炒菜时经常使用铁锅可以预防缺铁性贫血 | |
| D. | 亚硝酸钠可以代替食盐做食品的调味剂 |
4. 为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表
为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表
反应的化学方程式为(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl,其他成分能溶于水但不参加反应
(1)反应共生成BaSO4的质量为23.3g.
(2)若所取氨肥样品的质量为15g,试通过计算确定氨肥中硫酸铵的纯度是否与标签相符.(请写出计算过程)
(3)反应前后,溶液中硫元素的质量减小.(填“不变”、“增大”或“减小”)
 为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表
为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如表| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液总质量(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
(1)反应共生成BaSO4的质量为23.3g.
(2)若所取氨肥样品的质量为15g,试通过计算确定氨肥中硫酸铵的纯度是否与标签相符.(请写出计算过程)
(3)反应前后,溶液中硫元素的质量减小.(填“不变”、“增大”或“减小”)