题目内容
14.铁、铜等金属在我们的生活和工业生产中应用很广.某工厂利用废铁丝、硫酸铜废液(含硫酸亚铁)和废铜粉制备硫酸铜晶体.具体过程如下:
(1)将废铁丝投入到硫酸铜废液里发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu;反应类型为置换反应.(填基本反应类型)
(2)操作Ⅰ的名称是过滤.
(3)在氧化铜(含少量铜)转化为硫酸铜溶液的过程中,下列化学反应不可能发生的是C.(填序号)
A.2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO B.2Cu+O2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O
C.Cu+H2SO4═CuSO4+H2↑ D.CuO+H2SO4═CuSO4+H2O.
分析 根据金属活动性顺序的意义进行分析,在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,金属氧化物能与酸反应生成盐和水.
解答 解:(1)铁在铜的前面,能将硫酸铜中的铜置换出来,反应的方程式为:Fe+CuSO4=FeSO4+Cu,该反应是单质和化合物反应产生新的单质和化合物,属于置换反应;
(2)铁在氢的前面能与酸反应,而铜不与酸反应,多余的铁可以与酸反应除去,然后通过过滤得到铜粉;
(3)铜能与氧气反应生成氧化铜,氧化铜能与酸反应生成铜盐和水,而铜不能和硫酸反应,因此错误的是C.
故答案为:(1)Fe+CuSO4=FeSO4+Cu; 置换;(2)过滤; (3)C.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
5.如图是某个化学反应的微观示意图,从示意图中获取的信息不正确的是( )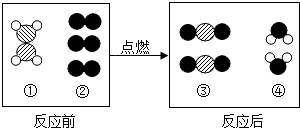

| A. | 图①分子中两种原子的个数比为1:2 | B. | 图②对应的物质是单质 | ||
| C. | 反应前后原子的种类和个数不变 | D. | 两种生成物的分子个数比为1:2 |
9. 全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )
全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )
 全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )
全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )| A. | 水银的化学式为Hg | B. | 汞原子的质量为200.6g | ||
| C. | 汞原子的中子数是80 | D. | 汞为非金属元素 |
19.下列生活用品所使用的主要材料,属于有机合成材料的是( )
| A. |  青花瓷瓶 | B. |  橡胶轮胎 | C. |  真丝围巾 | D. |  羊毛衫 |
6.“生活中处处有化学”,下列说法中错误的是( )
| A. | 进到花园能闻到花香,说明分子在不断的运动 | |
| B. | 食用加碘盐,能预防甲状腺肿大疾病 | |
| C. | 打开啤酒瓶盖,啤酒会自动溢出:是因为在温度不变时压强减小,气体溶解度也较小 | |
| D. | 在生铁和钢中,因钢中含碳量高,所以应用广泛:可做炊具和医疗器具 |
3.分类是化学学习和研究的重要方法之一,下列分类中正确的是( )
| A. | 碳铵、尿素、硝酸铵都是氮肥 | B. | 空气、冰水、碘酒都是混合物 | ||
| C. | 烧碱、纯碱、熟石灰都是碱 | D. | 黄铜、铁红、不锈钢都是合金 |
4.酸都有一些相似的化学性质是由于( )
| A. | 酸溶液中都含有酸根离子 | B. | 酸溶液pH<7 | ||
| C. | 酸溶液中阳离子都是H+ | D. | 酸溶液都能使紫色石蕊溶液变红 |
 的垃圾箱中的是ABC(填字母序号).
的垃圾箱中的是ABC(填字母序号).