题目内容
7. 西园中学化学兴趣小组在老师指导下,对碳酸钠、碳酸氢钠的性质作进一步探究.
西园中学化学兴趣小组在老师指导下,对碳酸钠、碳酸氢钠的性质作进一步探究.Ⅰ.探究碳酸钠、碳酸氢钠的热稳定性
【实验过程】
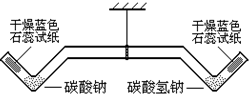
(1)截取一根长短合适的玻璃管,利用酒精喷灯将其加工成长柄双V管.
(2)按如图所示,装好药品和试纸,确保长柄双V管处于水平的平衡状态.
(3)以下操作不考虑空气的干扰.
| 实验现象 | 实验结论 | |
| ①用酒精灯加热左端的碳酸钠2min | 长柄双V管保持水平,干燥的蓝色石蕊试纸不变色 | 碳酸钠受热不分解 |
| ②再加热右端的碳酸氢钠2min | 长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色 | 碳酸氢钠受热分解成碳酸钠等物质,有关的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ |
(4)碳酸钠俗称苏打、纯碱等,常用作洗涤剂.
(5)碳酸氢钠俗称小苏打,常用于发酵粉、治疗胃酸过多等.
Ⅱ.探究碳酸氢钠受热后残留的白色固体成分
【作出猜想】
同学们猜想碳酸氢钠受热后,残留的白色固体成分可能是:
①全部是碳酸氢钠;②全部是碳酸钠;③碳酸氢钠和碳酸钠的混合物.
老师指出,猜想①无需验证,就知道不合理,因为长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色,说明碳酸氢钠受热分解为碳酸钠、水和二氧化碳;不可能全部是碳酸氢钠.
【查阅资料】
碳酸氢钠溶于水吸收热量,碳酸钠溶于水放出热量.
【设计方案】
同学们设计出下列3个实验方案,其中正确的是B(填序号).
A.将残留的白色固体溶于水,若有放热现象,则猜想②正确
B.加热一定量残留的白色固体,若质量减轻,则猜想③正确
C.向残留的白色固体中滴加稀盐酸,若有气泡产生,则猜想②正确.
分析 根据碳酸氢钠受热分解成碳酸钠等物质,写出有关的化学方程式;
Ⅰ.(4)根据碳酸钠俗称解答;
(5)根据碳酸氢钠的作用解答;
Ⅱ.根据碳酸氢钠受热后,残留的白色固体成分可能是:①全部是碳酸氢钠;②全部是碳酸钠;③碳酸氢钠和碳酸钠的混合物解答;
根据长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色解答;
解答 解:
用酒精灯加热左端的碳酸钠2min,长柄双V管保持水平,干燥的蓝色石蕊试纸不变色,说明碳酸钠受热不分解;
碳酸氢钠受热分解成碳酸钠等物质,有关的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
Ⅰ.(4)碳酸钠俗称苏打、纯碱等,常用作洗涤剂.
(5)碳酸氢钠俗称小苏打,常用于发酵粉、治疗胃酸过多等;
Ⅱ.碳酸氢钠受热后,残留的白色固体成分可能是:①全部是碳酸氢钠;②全部是碳酸钠;③碳酸氢钠和碳酸钠的混合物;
长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色,说明碳酸氢钠受热分解为碳酸钠、水和二氧化碳;不可能全部是碳酸氢钠;
【设计方案】
碳酸氢钠溶于水吸收热量,碳酸钠溶于水放出热量.
A、将残留的白色固体溶于水,若有放热现象,可能是碳酸钠或碳酸氢钠和碳酸钠的混合物,故错误;
B、加热一定量残留的白色固体,若质量减轻,说明有碳酸氢钠,则猜想③正确,故正确;
C、向残留的白色固体中滴加稀盐酸,若有气泡产生,碳酸钠或碳酸氢钠和碳酸钠的混合物都能出现此现象,故错误.
答案:
Ⅰ.
| 实验现象 | 实验结论 | |
| ①用酒精灯加热左端的碳酸钠2min | 长柄双V管保持水平,干燥的蓝色石蕊试纸不变色 | 碳酸钠受热 不分解 |
| ②再加热右端的碳酸氢钠2min | 长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色 | 碳酸氢钠受热分解成碳酸钠等物质,有关的化学方程式是 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ |
(5)发酵粉、治疗胃酸过多等;
Ⅱ.【作出猜想】碳酸氢钠和碳酸钠的混合物;
长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色,说明碳酸氢钠受热分解为碳酸钠、水和二氧化碳;不可能全部是碳酸氢钠;
【设计方案】B.
点评 掌握碳酸盐和酸反应放出二氧化碳气体,酚酞试液的变色情况、方程式的书写,以及碳酸钠、氢氧化钠的性质,是解答的基础和关键,此外,该题还较好的考查了学生根据题意分析解决问题、应用知识解决问题的能力.

练习册系列答案
相关题目
14.下列说法中,正确的是( )
| A. | 家用电器着火,立即用水泼灭 | |
| B. | 日常生活中,用生石灰做干燥剂 | |
| C. | 发令枪中红磷燃烧时产生大量“白雾” | |
| D. | 生铁和钢都是铁合金,在用途上没有区别 |
18.下列有关推理中,正确的是( )
| A. | 复分解反应生成两种化合物,则生成两种化合物的反应一定是复分解反应 | |
| B. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| C. | 有机物都含碳元素,所以含碳元素的化合物一定是有机物 | |
| D. | 酸性溶液能使石蕊溶液变红,则使石蕊溶液变红的一定是酸性溶液 |
15.下列方法不能把待鉴别的物质区分开的是( )
| 选项 | 待鉴别的物质 | 鉴别方法 |
| A | 氯化钾和碳酸钡固体 | 水 |
| B | 稀硫酸和氯化钠溶液 | 加酚酞 |
| C | Cu粉与CuO粉末 | 稀硫酸 |
| D | 棉纤维、羊毛纤维 | 点燃,闻燃烧产生的气味 |
| A. | A | B. | B | C. | C | D. | D |
12.科学史上每一次重大发现都极大地推进了科学的发展,俄国科学家门捷列夫对化学突出贡献在于( )
| A. | 提出了元素周期律 | |
| B. | 首次较准确的测定了空气中氧气的体积含量 | |
| C. | 揭示了燃烧的本质 | |
| D. | 提取了治疟药物青蒿素 |
19.央视3•15晚会曝光,检测机构检验后发现市场上修正液的主要溶剂为三氯乙烷(化学式为C2H3O3).下列对三氯乙类烷的说法正确的是( )
| A. | 三氯乙烷中碳元素与氢元素的质量比为8:1 | |
| B. | 三氯乙烷的相对分子质量为133.5g | |
| C. | 三氯乙烷是无机物 | |
| D. | 三氯乙烷由4种元素组成 |
16.化学课上老师要求同学们利用一种试剂鉴别出三种无色溶液,它们是NaOH、AgNO3、KNO3溶液中的一种.所用的这种试剂是( )
| A. | 铁粉 | B. | FeCl3溶液 | C. | NaCl溶液 | D. | Na2CO3溶液 |