题目内容
4.某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.【查阅资料】
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
(1)探究两者水溶液酸碱性的差异小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变红色,比较两种溶液的碱性强弱,可直接用pH试纸进行测定.
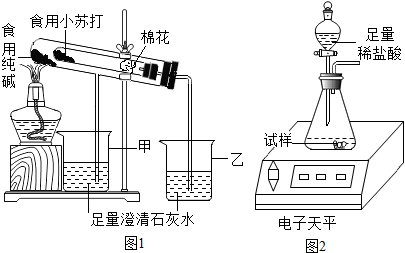
(2)验证两种粉末的稳定性在老师的指导下,该小组按图1装置进行实验操作,观察到乙(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,装置中棉花的作用是防止加热时小苏打粉末进入导管.
(3)测定食用纯碱粉末的纯度取食用纯碱粉末试样,利用图2装置进行实验测定.数据记录如下:
| 称量项目 | 称量时间 | 电子天平试样足量稀盐酸 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
②通过计算确定食用纯碱粉末中Na2CO3的质量分数.(写出计算过程,结果保留一位小数)
分析 根据已有的知识进行分析,酚酞试液在碱性溶液中为红色,碱性溶液的pH越大,碱性越强;碳酸氢钠在加热时能分解生成碳酸钠、水和二氧化碳,根据碳酸钠与盐酸反应的质量变化,即可求出生成二氧化碳的质量以及计算碳酸钠的质量分数,据此解答即可.
解答 解:(1)食用纯碱以及碳酸氢钠的水溶液都呈碱性,能使酚酞试液变红,测定溶液的pH可以使用pH试纸,故填:红,食用纯碱,pH试纸;
(2)碳酸氢钠受热能分解生成碳酸钠、水和二氧化碳,而碳酸钠受热不分解,故乙烧杯中的石灰水会变浑浊,在试管口放一团棉花能防止加热碳酸氢钠时其粉末随气流进入导管,故填:乙,防止加热时小苏打粉末进入导管;
(3)碳酸氢钠能与盐酸反应,可以用于治疗胃酸过多,故填:治疗胃酸过多;
(4)①生成二氧化碳的质量为:11.0g+160g-166.6g=4.4g,故填:4.4.
②设生成4.4g二氧化碳需要碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$
x=10.6g
食用纯碱粉末中Na2CO3的质量分数为:$\frac{10.6g}{11.0g}$≈96.4%
故填:食用纯碱粉末中Na2CO3的质量分数96.4%;
点评 本题考查了碳酸钠的性质以及有关的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
15.下列各组物质的溶液不用其他试剂就可鉴别出来的是( )
| A. | HCl CuCl2 NaNO3 Na2SO4 | B. | BaCl2 Na2CO3 HCl (NH4)2CO3 | ||
| C. | FeCl3 HCl NaCl NaOH | D. | Na2CO3 Na2SO4 HCl H2SO4 |
19.下列说法正确的是( )
| A. | 物质和氧气发生的反应一定属于化合反应 | |
| B. | 化学式CO2可以代表一个二氧化碳分子,也可以代表二氧化碳这种物质 | |
| C. | 原子一定是由质子、中子、电子构成的 | |
| D. | pH>7的溶液一定是碱的溶液 |
13.下列数据为常见水果的近似pH,其中酸性最强的是( )
| A. | 杨梅pH=2.5 | B. | 苹果pH=4.1 | C. | 菠萝pH=5.1 | D. | 柿子pH=8.5 |
14.下列模型能表示氧气分子结构的是( )
| A. | 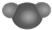 | B. |  | C. | 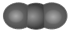 | D. | 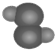 |
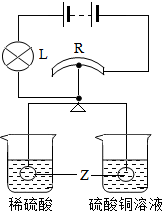 如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠杆的中央且可以随杠杆左右移动.杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将锌球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到:
如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠杆的中央且可以随杠杆左右移动.杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将锌球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到: