题目内容
20.向8.9g氯化铜和氯化钠的混合物加入一定量溶质质量分数为8%的氢氧化钠溶液恰好完全反应后过滤,得到4.9g沉淀,向滤液中加入一定量水得到溶质质量分数为5%的溶液.计算:(1)所加氢氧化钠溶液的质量;(2)向滤液中加入水的质量是多少?
分析 (1)根据氢氧化钠和氯化铜会生成氢氧化铜沉淀和氯化钠,依据沉淀的质量计算参加反应的氢氧化钠的质量;
(2)根据化学方程式计算生成氯化钠的质量,依据反应后溶液的溶质质量分数计算加入水的质量.
解答 解:(1)设加入氢氧化钠的溶液质量为x,生成氯化钠的质量为y,混合物中氯化铜的质量为z
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
135 80 98 117
z x×8% 4.9g y
$\frac{80}{x×8%}$=$\frac{98}{4.9g}$=$\frac{117}{y}$=$\frac{135}{z}$
x=50g
y=5.85g
z=6.75g
(2)向滤液中加入水的质量是:$\frac{5.85g+8.9g-6.75g}{5%}$-50g×(1-8%)=114g.
故答案为:(1)50g;
(2)114g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
相关题目
10.某科研所成功利用染化厂的废料铁泥(主要成分是Fe2O3、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁.
(1)在物质分类中,四氧化三铁属于氧化物(填写物质类别).
(2)制备过程中要用到双氧水(过氧化氢溶液),其中双氧水溶液的用量、调节的pH、反应时间是三个关键条件,研究时需要进行七组对比实验.若实验序号1是该制备过程的理论最佳制备条件,请在下表中完善实验序号为7的实验条件(与1-6组实验条件不同).
(3)调节溶液的pH可用碳酸钠或碳酸氢钠.
查阅资料可知:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,此反应的基本类型是分解反应反应,此反应证明NaHCO3的热稳定性小于 Na2CO3(填“大于”或“小于”).
请你根据以上性质设计实验方案鉴别Na2CO3和NaHCO3固体.分别取两种适量固体于两试管中,分别加热,并将可能生成的气体通入澄清石灰水中,如有白色沉淀生成,则该试管中是NaHCO3.
试写出实验方案中另一个化学反应方程式Ca(OH)2+CO2=CaCO3↓+H2O.
(1)在物质分类中,四氧化三铁属于氧化物(填写物质类别).
(2)制备过程中要用到双氧水(过氧化氢溶液),其中双氧水溶液的用量、调节的pH、反应时间是三个关键条件,研究时需要进行七组对比实验.若实验序号1是该制备过程的理论最佳制备条件,请在下表中完善实验序号为7的实验条件(与1-6组实验条件不同).
| 实验序号 | 双氧水溶液(mL) | pH | 反应时间(h) |
| 1 | 6 | 10 | 3 |
| 2 | 5 | 10 | 3 |
| 3 | 6 | 11 | 3 |
| 4 | 6 | 10 | 2 |
| 5 | 7 | 10 | 3 |
| 6 | 6 | 9 | 3 |
| 7 | 6 | 10 | 4(大于3即可) |
查阅资料可知:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,此反应的基本类型是分解反应反应,此反应证明NaHCO3的热稳定性小于 Na2CO3(填“大于”或“小于”).
请你根据以上性质设计实验方案鉴别Na2CO3和NaHCO3固体.分别取两种适量固体于两试管中,分别加热,并将可能生成的气体通入澄清石灰水中,如有白色沉淀生成,则该试管中是NaHCO3.
试写出实验方案中另一个化学反应方程式Ca(OH)2+CO2=CaCO3↓+H2O.
11.如表整理的与化学有关的知识不完全正确的是( )
| A | 食品保鲜的办法 | B | 灭火实例与原理 |
| 用甲醛泡制海鲜-防腐保鲜 放入生石灰--防止受潮 | 油锅着火时用锅盖盖灭-隔绝空气 住宅失火时用水灭火--降低着火点 | ||
| C | 日常物质的区别 | D | 化学中常见的“三” |
| 硬水和软水--加肥皂水并搅拌 聚乙烯和聚氯乙烯--点燃闻气味 | 三种可燃性气体-H2、CO、CH4 三种构成物质的粒子--分子、原子、离子 |
| A. | A | B. | B | C. | C | D. | D |
9.下表列出了除去物质中所含少量杂质的方法,其中不正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 氧化铜 | 铜 | 在空气中充分加热 |
| B | 氧化钙 | 碳酸钙 | 充分高温煅烧 |
| C | 氮气 | 二氧化碳 | 先通过足量的氢氧化钠溶液,后通过足量浓硫酸 |
| D | 硫酸钠溶液 | 碳酸氢钠 | 加入适量的稀硫酸、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
10.一些食物的近似PH如下:其中显碱性的是( )
| A. | 鸡蛋清:7.6~8.0 | B. | 葡萄汁:3.5~4.5 | C. | 牛奶:6.3~6.6 | D. | 苹果汁:2.9~3.3 |

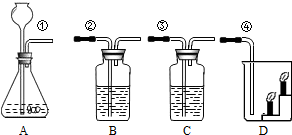 实验室按如图所示装置制取CO2,并检验CO2的性质,试回答以下问题:
实验室按如图所示装置制取CO2,并检验CO2的性质,试回答以下问题: