题目内容
14.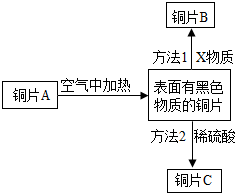 图为铜片A的系列变化,据图回答问题:
图为铜片A的系列变化,据图回答问题:(1)若方法1中的X物质为常见气体,且发生置换反应,则X是H2(填化学式);
(2)写出方法2的化学方程式CuO+H2SO4=CuSO4+H2O;
(2)铜片A、铜片B、铜片C的质量分别为mA、mB、mC,其中方法1和方法2均完全反应,则mA、mB、mC的大小关系为mA=mB>mC.
分析 (1)根据常见的还原剂有碳单质、一氧化碳和氢气,X物质为常见气体,且发生置换反应,所以X是氢气进行分析;
(2)根据氧化铜和硫酸反应生成硫酸铜和水进行分析;
(3)根据方法1是将已经部分氧化的铜片重新用氢气还原,依据质量守恒中的原子守恒,方法1反应结束后,铜被重新还原,所以mA=mB,方法2中部分氧化的铜片产生了氧化铜,氧化铜与硫酸反应,有部分铜元素进入溶液中,剩余的铜单质的质量为mC,所以小于mA、mB进行分析.
解答 解:(1)常见的还原剂有碳单质、一氧化碳和氢气,X物质为常见气体,且发生置换反应,所以X是氢气,化学式为:H2;
(2)氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4=CuSO4+H2O;
(3)方法1是将已经部分氧化的铜片重新用氢气还原,依据质量守恒中的原子守恒,方法1反应结束后,铜被重新还原,所以mA=mB,方法2中部分氧化的铜片产生了氧化铜,氧化铜与硫酸反应,有部分铜元素进入溶液中,剩余的铜单质的质量为mC,所以小于mA、mB,所以mA、mB、mC的大小关系为mA=mB>mC.
故答案为:(1)H2;
(2)CuO+H2SO4=CuSO4+H2O;
(3)mA=mB>mC.
点评 本题主要考查了金属的化学性质和化学方程式的书写,难度不大,需要在平时加强记忆即可完成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.a、b、c三种酸分别与足量的金属Mg充分反应,生成等质量H2,的反应消耗a、b、c的分子数目之比为3:6:2,下列关于a、b、c的推理合理的是(HX、H2Y、H3Z分别表示三种酸)( )
| A. | a、b、c三种酸溶液中的H原子数目:c>a>b | |
| B. | a、b、c可能分别为H2Y、HX、H3Z | |
| C. | a、b、c的相对分子质量:b<a<c | |
| D. | a、b、c与金属Mg反应的速率:b>a>c |
2.某气体由CH4、C2H4、C2H2中的一种或几种组成,取气体样品在氧气中完全燃烧,测得生成的二氧化碳和水的质量比为22:9,下列对该气体组成的判断正确的是( )
| A. | 该气体可能是由C2H4和C2H2组成 | |
| B. | 该气体一定含有C2H4 | |
| C. | 该气体中可能含有CH4 | |
| D. | 该气体不可能同时含有CH4、C2H4、C2H2 |
19.为了验证金属的活动性,同学们将洁净的铁钉放入硫酸铜溶液中,观察到铁钉表面变为红色,反应的化学方程式为Fe+CuSO4═FeSO4+Cu;.细心的同学发现,铁钉表面同时含有气泡冒出,就此气泡成分,同学们在老师指导下进行了如下探究:
【提出猜想】
同学们一致认为C同学的猜想是不合理的,理由是根据质量守恒定律,化学反应前后元素种类不变,反应物中没有碳元素所以生成物中一定没有二氧化碳.
【查阅资料】二氧化硫具有漂白性,会使品红溶液褪色.
【进行实验】利用如图所示的装置分别进行实验
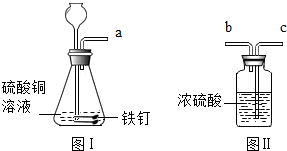
(1)反应一段时间后,A同学将带火星的木条放在a处,观察到带火星的木条没有复燃,则她的猜想错误.
(2)B同学将产生的气体通入品红溶液中,观察到品红溶液不褪色,则她的猜想也错误.
(3)D同学将图Ⅰ中的a端导管与图Ⅱ中的c端导管相连,目的是对其他进行干燥.反应一段时间后,点燃从图Ⅱ另一端导管出来的气体,通过对现象的分析,得出他的猜想正确.
【得出结论】铁与硫酸铜溶液反应时伴随产生了氢气.
【讨论反思】这几位同学的实验方案存在安全隐患,理由是该实验中氢气属于可燃性气体,不纯点燃可能会发生爆炸,改进的方法是先将从a处的气体通入图Ⅱ一段时间后再点燃.
【继续追问】铁与硫酸铜溶液反应为什么会伴随产生氢气?
【查阅资料】有些盐在水溶液中会发生水解反应,使盐溶液不一定呈中性.
【再次猜想】硫酸铜溶液可能显酸性.
【验证方案】
【反思与评价】同学们做完以上实验很有成就感,体验到探究的快乐,并感慨“科学探究无止境”!
【提出猜想】
| 同学 | A | B | C | D |
| 对气泡成分的猜想 | 氧气 | 二氧化硫 | 二氧化碳 | 氢气 |
【查阅资料】二氧化硫具有漂白性,会使品红溶液褪色.
【进行实验】利用如图所示的装置分别进行实验

(1)反应一段时间后,A同学将带火星的木条放在a处,观察到带火星的木条没有复燃,则她的猜想错误.
(2)B同学将产生的气体通入品红溶液中,观察到品红溶液不褪色,则她的猜想也错误.
(3)D同学将图Ⅰ中的a端导管与图Ⅱ中的c端导管相连,目的是对其他进行干燥.反应一段时间后,点燃从图Ⅱ另一端导管出来的气体,通过对现象的分析,得出他的猜想正确.
【得出结论】铁与硫酸铜溶液反应时伴随产生了氢气.
【讨论反思】这几位同学的实验方案存在安全隐患,理由是该实验中氢气属于可燃性气体,不纯点燃可能会发生爆炸,改进的方法是先将从a处的气体通入图Ⅱ一段时间后再点燃.
【继续追问】铁与硫酸铜溶液反应为什么会伴随产生氢气?
【查阅资料】有些盐在水溶液中会发生水解反应,使盐溶液不一定呈中性.
【再次猜想】硫酸铜溶液可能显酸性.
【验证方案】
| 操作 | 现象 | 结论 |
| 向硫酸铜溶液中滴加石蕊试液 | 溶液变红 | [再次猜想]是正确的. |
6.如图所示的实验装置或实验操作正确的是( )
| A. | 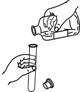 倾倒液体 | B. |  闻气体的气味 | C. |  加热液体 | D. | 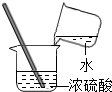 稀释浓硫酸 |
3.下列化肥中属于复合肥料的是( )
| A. | Ca3(PO4)2 | B. | (NH4)2SO4 | C. | KH2PO4 | D. | CO(NH2)2 |
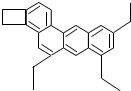 化学家Tim Richard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26).请计算:
化学家Tim Richard将分子结构简式像小狗的某有机物(如图所示),取名为“小狗烯”(化学式为C26H26).请计算:


