题目内容
3.如图是八年级化学中常见的实验装置图.请回答下列问题: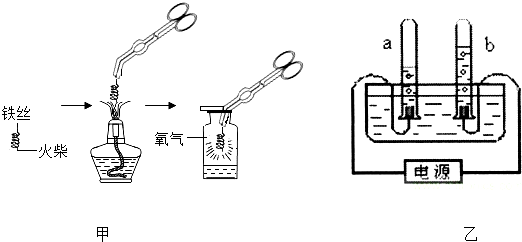
(1)甲图中铁丝在氧气中燃烧的现象是剧烈燃烧、火星四射、生成黑色固体、放出大量的热,该反应的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,反应的基本类型是化合反应.
(2)做铁丝在氧气中燃烧的实验时,通常把铁丝绕城螺旋状的目的是增大铁丝与氧气的接触面积,在集气瓶底部铺一层细沙或盛放少量水的目的是防止高温生成物炸裂集气瓶底部.
(3)另一组的同学,用实验桌上的一瓶氧气做该实验时,没有看到铁丝燃烧时的现象发生,请分析实验失败的原因是铁丝未用砂纸打磨、氧气浓度不高.
(4)乙图是电解水实验,a试管中产生的气体是H2(填化学式),a、b两支试管中产生气体的体积比是2:1,写出该反应的文字表达式水$\stackrel{通电}{→}$氢气+氧气;该实验验证了水是由氢元素和氧元素组成的,还揭示了化学变化的实质:在化学变化中分子可以再分,而原子不能再分.
分析 (1)从铁丝在氧气中燃烧的现象、化学方程式、反应类型去分析;
(2)从做铁丝在氧气中燃烧的实验时的注意事项去分析;
(3)从做铁丝在氧气中燃烧实验时的注意事项去分析;
(4)从给水通电的实验现象及结论去分析.
解答 解:(1)铁丝在氧气中燃烧的现象是剧烈燃烧、火星四射、生成黑色固体(四氧化三铁),其反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;由于反应物是两种,生成物是一种,所以属于化合反应;故答案为:火星四射 生成黑色固体 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 化合反应;
(2)做铁丝在氧气中燃烧的实验时,通常把铁丝绕城螺旋状的目的是增大铁丝与氧气的接触面积;在集气瓶底部铺一层细沙或盛放少量水的目的是防止高温生成物炸裂集气瓶底部;故答案为:增大铁丝与氧气的接触面积、防止高温生成物炸裂集气瓶底部;
(3)做铁丝在氧气中燃烧实验时,如铁丝未用砂纸打磨,铁丝表面的铁锈会阻止铁丝与氧气的接触,导致实验失败;如果氧气浓度不高,铁丝也不会燃烧;故答案为:铁丝未用砂纸打磨 氧气浓度不高;
(4)给水通电时,试管内的电极上出现气泡,过一段时间,与电源正(氧气),负极(氢气)相连的试管产生的气体体积比约为1:2.其反应的文字表达式为:水$\stackrel{通电}{→}$氢气+氧气;由图中可以看出a管中产生的气体较多,故是氢气;由于生成的氢气是由氢元素组成的,氧气是由氧元素组成的,根据质量守恒定律,反应前后元素的种类不变,可推出水是由氢元素和氧元素组成的;从微观的在变化过程中水分子分成氢原子和氧原子,氢原子和氧原子通过重新组合为新的分子--氢分子和氧分子,从而证明了在化学变化中分子可以再分而原子不能;
故答案为:H2 2:1 氢元素和氧元素 分子 原子.
点评 本题主要考查了有关铁丝在氧气中燃烧实验的现象及注意事项、电解水的实验现象、化学方程式及结论等,难度不大,基础性较强.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 纸燃烧化为灰烬,灰烬的质量比纸的质量小 | |
| B. | 镁条燃烧,生成物的质量比镁条的质量大 | |
| C. | 5g 蔗糖溶于95g水中,溶液总质量为100g | |
| D. | 高锰酸钾受热后,固体质量减少 |
| A. | 该气体一定是纯净物 | B. | 该气体一定是CO、CO2的混合物 | ||
| C. | 该气体中所含的物质最多只有2种 | D. | 该气体的组成情况最多3种 |
| A. | 锌粒和盐酸 | B. | 锈铁钉和稀硫酸 | ||
| C. | 二氧化碳与石灰水 | D. | 二氧化碳与氢氧化钠溶液 |
| A. | 蒸发水 | B. | 食盐溶解 | C. | 矿石粉碎 | D. | 铁生锈 |
①除去热水瓶中的水垢 ②鉴别氯化钠与碳酸钠
③检验鸡蛋壳是否有碳酸盐 ④测定雨水的酸碱度.
| A. | ①④ | B. | ③④ | C. | ①②③ | D. | ①②③④ |