题目内容
11. 实验室中有一瓶长期放置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.
实验室中有一瓶长期放置的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行探究.[发现问题]该样品中含有哪些物质?
[查阅资料]①NaOH在空气中不会转化成NaHCO3.
②BaCl2溶液呈中性,Ba(OH)2是可溶性强碱.
③CO2在饱和的NaHCO3溶液中几乎不溶解.
[提出猜想]猜想Ⅰ:NaOH;
猜想Ⅱ:Na2CO3;
猜想Ⅲ:NaOH和Na2CO3.
[设计实验]
| 实验操作 | 实验现象 |
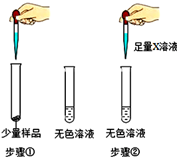 | 步骤①:样品全部溶解 步骤②:观察到现象A |
(1)若现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅰ(填“猜想Ⅰ”、“猜想Ⅱ”或“猜想Ⅲ”)不成立.
(2)若X溶液为BaCl2溶液,现象A是有白色沉淀生成,则产生该沉淀的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl.取反应后的上层清液,测定其pH,当pH> 7(填“>”、“<”或“=”),则证明猜想Ⅲ成立.
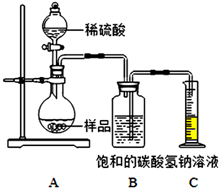
[定量分析]确定部分变质样品中Na2CO3的质量分数.兴趣小组的同学用如图所示装置进行实验.
步骤如下:
①按图连接好装置,并检查气密性;
②准确称取该样品1.0g,放入烧瓶内;
③打开活塞,滴加30.0%的稀硫酸至过量,关闭活塞.
④反应结束后,量筒内液体读数为55.0mL.
(已知:室温条件下,CO2的密度约为1.6g•L-1)
(1)B装置集气瓶内原有的空气对实验结果没有(填“有”或“没有”)影响.饱和碳酸氢钠溶液如果用水代替,则所测CO2的体积偏小(填“偏大”、“偏小”或“不变”),理由是二氧化碳会与水反应,易溶于水.
(2)计算该固体样品中Na2CO3的质量分数21.2%.(计算结果保留一位小数)
[实验反思]证明猜想Ⅲ是否成立,实验操作中的X溶液为BaCl2溶液,还可以改为滴加氯化钙溶液;取反应后的上层清液,除了测定其pH外,还可以滴加酚酞溶液.
分析 【收集证据】(1)根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳进行分析;
(2)根据氯化钡和碳酸钠会生成碳酸钡沉淀和氯化钠,以及猜想Ⅲ中含有碳酸钠、氢氧化钠进行分析;
【定量分析】(1)根据二氧化碳在空气中的含量进行分析;
根据二氧化碳会与水反应,易溶于水进行分析;
根据碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,结合题中的数据进行解答;
【实验反思】根据氯化钙与碳酸钠反应生成沉淀、考虑碱与酚酞的变色规律,进行分析.
解答 解:【收集证据】(1)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,所以现象A是有气泡产生,则X溶液为稀盐酸,则猜想Ⅰ成立;
(2)氯化钡和碳酸钠会生成碳酸钡沉淀和氯化钠,化学方程式为:BaCl2+Na2CO3═BaCO3↓+2NaCl,猜想Ⅲ中含有碳酸钠、氢氧化钠,所以取反应后的上层清液,测定其pH>7;
【定量分析】(1)空气中含有的二氧化碳量很少,不会对结果产生大的影响;
二氧化碳会与水反应,易溶于水,所以饱和NaHCO3溶液如果用水代替,则所测CO2体积偏小;
设参加反应的碳酸钠是X,
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 44
x 55mL×1.6g/L
$\frac{106}{x}$=$\frac{44}{55mL×1.6g/L}$,解得x=0.212g.
所以该样品中Na2CO3的质量分数为:$\frac{0.212g}{1g}$×100%=21.2%;
【实验反思】证明猜想Ⅲ是否成立,实验操作中的X溶液为BaCl2溶液,还可以改为滴加氯化钙溶液;取反应后的上层清液,除了测定其pH外,还可以滴加酚酞溶液.
故答案为:
【收集证据】(1)稀盐酸,猜想Ⅰ;(2)BaCl2+Na2CO3═BaCO3↓+2NaCl,>;
【定量分析】(1)没有;偏小;21.2%;【实验反思】氯化钙; 酚酞.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.解这类题目时,选择试剂很重要,要注意在检验和除杂的不同,在除去杂质的同时,原物质不能减少,但可以增多,且反应后不能生成新的杂质.

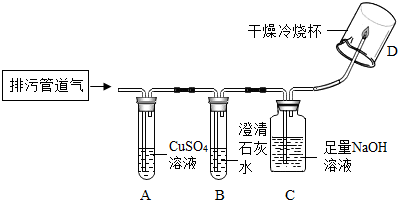
| A. | 干冰挥发出大量的水蒸气 | |
| B. | 干冰挥发出大量的白色二氧化碳气体 | |
| C. | 干冰被空气中的氧气氧化产生了大量的白色气体 | |
| D. | 干冰升华吸收了大量的热,使周围温度降低,大量的水蒸气凝结成了小液滴 |
| A. | 冬天用煤炉取暖时关紧门窗 | |
| B. | 进入古井前,应先做灯火试验 | |
| C. | 塑料袋方便又经济,应提倡使用 | |
| D. | 油锅不慎着火,立即用大量的水冲灭 |
| A. | 倒入废液缸 | B. | 交回实验室集中处理 | ||
| C. | 放回原试剂瓶 | D. | 投入通向下水道的水槽内 |
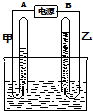 如图:
如图:
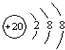 表示的是(写粒子符号)Ca2+.
表示的是(写粒子符号)Ca2+.