题目内容
(2013?广州)Na2SO4是常用的化工原料,下列说法正确的是( )
分析:A、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
B、根据化合物中元素的质量分数=
×100%,进行分析判断.
C、硫酸钠溶液是硫酸钠的水溶液,硫酸钠是由钠离子和硫酸根离子构成的,水是由水分子构成的.
D、根据硫酸钠溶液中存在能自由移动的离子进行分析判断.
B、根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
C、硫酸钠溶液是硫酸钠的水溶液,硫酸钠是由钠离子和硫酸根离子构成的,水是由水分子构成的.
D、根据硫酸钠溶液中存在能自由移动的离子进行分析判断.
解答:解:A、Na2SO4中钠、硫、氧三种元素的质量比为(23×2):32:(16×4)≠2:1:4,故选项说法错误.
B、Na2SO4中S元素的质量分数为
×100%,故选项说法错误.
C、硫酸钠溶液是硫酸钠的水溶液,硫酸钠是由钠离子和硫酸根离子构成的,水是由水分子构成的,Na2SO4溶液含有钠离子、硫酸根离子和水分子,故选项说法错误.
D、硫酸钠溶液中存在能自由移动的钠离子、硫酸根离子,可以导电,故选项说法正确.
故选D.
B、Na2SO4中S元素的质量分数为
| 32 |
| 23×2+32+16×4 |
C、硫酸钠溶液是硫酸钠的水溶液,硫酸钠是由钠离子和硫酸根离子构成的,水是由水分子构成的,Na2SO4溶液含有钠离子、硫酸根离子和水分子,故选项说法错误.
D、硫酸钠溶液中存在能自由移动的钠离子、硫酸根离子,可以导电,故选项说法正确.
故选D.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算、溶液导电的原因等进行分析问题、解决问题的能力.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
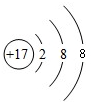 (2013?广州)如图是元素X的一种粒子结构示意图,下列说法正确的是( )
(2013?广州)如图是元素X的一种粒子结构示意图,下列说法正确的是( ) (2013?广州)某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Mg(NO3)2溶液、Ba(NO3)2溶液、Cu(NO3)2溶液、NaNO3溶液.
(2013?广州)某学习小组在如图所示的化学药品柜中发现一瓶标签模糊不清的无色溶液,已知这瓶溶液是以下5瓶溶液中的一种:HNO3溶液、Mg(NO3)2溶液、Ba(NO3)2溶液、Cu(NO3)2溶液、NaNO3溶液.