题目内容
8.下列实验方案中,合理的是( )| A. | 制取Cu(OH)2:将CuO与NaOH溶液混合 | |
| B. | 分离MgCl2和K2SO4的混合物:加水溶解、过滤、干燥 | |
| C. | 检验BaCl2中是否含有BaCO3:取样品,加稀盐酸看是否有气泡产生 | |
| D. | 除去CO2中的水蒸气和HCl气体:依次通过NaOH溶液和浓硫酸 |
分析 A、根据氧化铜和氢氧化钠不反应分析;
B、根据氯化镁和硫酸钾都易溶于水分析;
C、根据碳酸钡能够和盐酸反应产生二氧化碳气体分析;
D、根据氢氧化钠能够和二氧化碳、氯化氢都反应分析.
解答 解:A、氧化铜和氢氧化钠不反应,故方案不合理;
B、氯化镁和硫酸钾都易溶于水,因此不能通过过滤分离,故方案不合理;
C、碳酸钡能够和盐酸反应产生二氧化碳气体,而和氯化钡不反应,可以检验,故方案合理;
D、氢氧化钠能够和二氧化碳、氯化氢都反应,不符合除杂的原则,故方案不合理;
故选项为:C.
点评 解答本题的关键是要充分理解各种物质的性质,只有这样才能对问题做出正确的判断,另外需要注意的就是选用的除杂试剂不能与原有物质反应,反应后不能引入新的杂质.

练习册系列答案
相关题目
3.下列关于能源的开发与利用的说法错误的是( )
| A. | 煤燃烧时产生的一氧化碳是形成酸雨的主要气体之一 | |
| B. | 汽油是石油加工的产品,是常用的汽车燃料 | |
| C. | 天然气是比较清洁的能源,其主要成分是甲烷 | |
| D. | 氢气是未来生活中最理想的清洁能源 |
20.下列变化中,属于化学变化的是( )
| A. | 气态氧气通过降温加压变成淡蓝色液体 | |
| B. | 打开浓盐酸瓶盖,瓶口出现白雾 | |
| C. | 二氧化硫在空气中造成酸雨 | |
| D. | 霓虹灯管通电发光 |
17.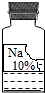 实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:
实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:
(1)【查阅资料】室温(20℃)时,四种物质的溶解度的数据如表:
【得出结论】某同学根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是上述溶液中的NaHCO3溶液.
(2)【设计实验】为了进一步确定该溶液是何种溶液,该同学进行了以下实验操作,请你帮助其补充完整下列实验方案,叙述实验操作、预期现象与结论.
 实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:
实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:(1)【查阅资料】室温(20℃)时,四种物质的溶解度的数据如表:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
(2)【设计实验】为了进一步确定该溶液是何种溶液,该同学进行了以下实验操作,请你帮助其补充完整下列实验方案,叙述实验操作、预期现象与结论.
| 实验操作 | 预期现象与结论 |
| 取少量样品溶液于试管中,滴加几滴酚酞试液. | 若无明显现象,则原溶液为NaCl 若溶液由无色变成红色,则原溶液为NaOH或Na2CO3 |
| 再取少量样品溶液于试管中,滴加少量稀盐酸. | 若试管中产生气泡,则原溶液为Na2CO3 若无明显现象,则原溶液为NaOH |