题目内容
元素是组成世界万物的基本成分,下列关于元素的说法不正确的是( )
|
| A. | 氯原子和氯离子都属于氯元素 |
|
| B. | 合金中一定含有金属元素 |
|
| C. | 人体缺铁元素会引起贫血 |
|
| D. | 碳和碘元素都是人体不可缺少的微量元素 |
| 元素的概念;合金与合金的性质;人体的元素组成与元素对人体健康的重要作用;矿物质与微量元素. | |
| 专题: | 物质的微观构成与物质的宏观组成. |
| 分析: | A.根据元素的概念来分析; B. C.根据人体健康与化学元素的关系来分析; D.根据人体需要的微量元素的种类来分析. |
| 解答: | 解:A.氯原子和氯离子都具有相同的质子数,属于同种元素,故正确; B.合金是在金属中加热熔合了其他金属或非金属而形成的具有金属特性的混合物,合金中一定含有金属元素,故正确; C.人体缺铁易患贫血症,故正确; D.碳元素属于人体所需的常量元素,故错误. 故选D. |
| 点评: | 本题考查的知识点较多,但是难度不大. |

 阅读快车系列答案
阅读快车系列答案PM2.5是指大气中直径≤2.5微米的颗粒物,是造成灰霾现象的罪魁祸首.下列措施不能有效减少PM2.5排放的是( )
|
| A. | 减少燃煤量,使用清洁能源 |
|
| B. | 控制机动车污染的排放,提升燃油品质 |
|
| C. | 多部门齐抓共管,减少扬尘污染 |
|
| D. | 建立区域联合机制,发布大气雾霾预警信号 |
某同学设计了以下三个实验,要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是( )
|
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
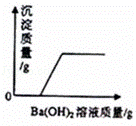
某溶液由NaOH、HCl、H2SO4和MgCl2中的一种或几种组成,向该溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液质量的关系如图,下列说法正确的是( )
|
| A. | HCl和H2SO4一定存在 |
|
| B. | NaOH、H2SO4和MgCl2一定不存在 |
|
| C. | HCl和MgCl2一定存在 |
|
| D. | HCl一定存在,NaOH、H2SO4一定不存在,MgCl2可能存在 |
某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
| R | O2 | CO2[来源:Z§xx§k.Com] | H2O | |
| 反应前质量(g) | 51 | 96 | 0 | 0 |
| 反应后质量(g) | x | 0 | 88 | 54 |
下列说法中不正确的是( )
A.x的值为5
B.R物质中只含有碳、氢元素
C.R物质中碳氢元素的质量比为4∶1
D.反应生成的二氧化碳和水的分子个数比为2∶3
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应 过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 、 。
(2)可以通过比较 实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。 。
 根据合金的组成来分析;
根据合金的组成来分析; X↑+2H2O X的化学式为 .
X↑+2H2O X的化学式为 .