题目内容
现有锌和另一种金属组成的合金6.5g,向此合金中加入100g一定溶质的质量分数的稀盐酸,充分反应后发现金属完全消失,若产生氢气的质量为m.则下列判断正确的是
A.如果合金为锌和铁,m不可能是0.2g
B.反应后溶液中的溶质一定只有两种
C.如果合金为锌和镁,m可能是0.1g,则该合金中锌的质量分数为50%
D.如果合金为锌和铁,所加稀盐酸的溶质的质量分数一定等于7. 3%
A
【解析】
试题分析:A、根据金属与酸反应产生氢气的质量=金属元素化合价绝对值/金属相对原子质量*金属质量可知,假设6.5g全部是锌的质量,则产生氢气的质量=2/65*6.5g=0.2g,假设6.5g全部是铁的质量,则产生氢气的质量=2/56*6.5g大于0.2g,所以若合金是锌和铁,则m不可能是0.2g,正确;B、若盐酸过量,则反应后的溶液中溶质除了两种金属与酸反应产生的盐外,还有HCl,错误;C、根据A可知,锌和镁产生氢气都大于或等于0.2g,则m不可能是0.1g,错误;D、若全部是锌,根据化学方程式进行计算得出盐酸的溶质质量分数为7.3%,若全部是铁,则盐酸的溶质质量分数大于7.3%,所以如果合金为铁和锌,所加稀盐酸溶质质量分数必然大于7.3%,错误。故选A
考点:物质成分的确定,金属化学性质。

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
 — 氧原子的结构示意图
— 氧原子的结构示意图
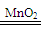 2H2O+O2↑ 分解反应
2H2O+O2↑ 分解反应 Ca(OH)2 化合反应
Ca(OH)2 化合反应 CaCO3 ↓+H2O 复分解反应
CaCO3 ↓+H2O 复分解反应 2Fe +3CO2 置换反应
2Fe +3CO2 置换反应