题目内容
9.如图甲是“△△牌发酵粉”的部分信息,课外化学兴趣小组的同学对其进行了如下探究(请你完成相应的填空)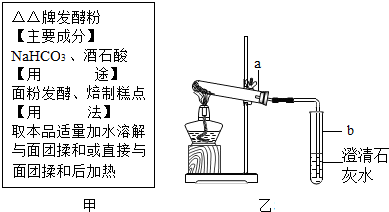
【查阅资料】
Ⅰ.酒石酸是一种易溶解于水的固体有机酸;
Ⅱ.发酵粉能够使面团松软、发泡是因为发酵粉产生了CO2所致;
Ⅲ.Na2CO3受热不分解.
【提出问题】
NaHCO3在发酵粉加水或加热时如何产生CO2?
【猜 想】
甲.…
乙.酒石酸与NaHCO3在溶液中反应产生CO2;
丙.NaHCO3加热产生CO2.
【实验探究】
①小明同学取少量NaHCO3粉末于试管中,加入适量水,无气体产生,从而否定了猜想甲,则猜想甲是NaHCO3与水反应产生CO2.小明又将酒石酸溶液和NaHCO3溶液混合,产生了CO2,从而验证了猜想乙,说明了NaHCO3具有的性质之一是NaHCO3与酒石酸能反应生成CO2.
②小英同学为探究猜想丙设计了如图乙所示的实验装置:小英另取适量粉末加入a试管中,加热,观察到a试管口有水生成,b试管中澄清石灰水变浑浊.试写出b试管中发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
持续加热直至两支试管均不再发生变化时,发现a试管中仍留有较多白色固体粉末,向该粉末中滴加稀盐酸,有CO2产生,说明该粉末是Na2CO3.
【小 结】
NaHCO3在发酵粉中产生CO2的条件是加水或加热;
NaHCO3受热发生变化的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 【实验探究】
①根据小明的实验操作以及实验结论来推测甲的实验猜想
根据小明的第二次操作过程,以及结论,得出碳酸氢钠的性质.
②能使澄清石灰水变浑浊的可能是二氧化碳气体,该气体又是碳酸氢钠加热的产物,推出反应方程式.
根据碳酸氢钠第一次加热后的产物和加入盐酸产生二氧化碳气体,确定粉末的成份.
【小 结】
根据以上的实验探究的结论,确定产生二氧化碳的条件.
根据反应物和生成物来书写化学反应方程式.
解答 解:【实验探究】
①依据小明在粉末中加水不会产生气体,来确定甲的猜想,故答案为:NaHCO3与水反应产生CO2.
酒石酸是一种易溶解于水的固体有机酸,将酒石酸溶液和NaHCO3溶液混合,产生了CO2,说明了酒石酸会与碳酸氢钠能反应生成气体,故答案为:NaHCO3与酒石酸能反应生成CO2.
②能使澄清石灰水变浑浊的可能是二氧化碳气体,该气体又是碳酸氢钠加热的产物,可以得出澄清石灰水变浑浊的方程式,故答案为:Ca(OH)2+CO2=CaCO3↓+H2O.
碳酸氢钠加热后生成了水和二氧化碳,根据质量守恒定律和加入盐酸后会产生气体,可以确定白色固体的化学式,故答案为:Na2CO3.
【小 结】
以上通过不同的探究实验分解验证了乙丙的猜想,故答案为:加水或加热.
根据碳酸氢钠在加热的条件下会生成水、二氧化碳和碳酸钠,故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
答案:
【实验探究】
①NaHCO3与水反应产生CO2.NaHCO3与酒石酸能反应生成CO2.
②Ca(OH)2+CO2=CaCO3↓+H2O.Na2CO3.
【小 结】
加水或加热.
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 本题通过不同的实验探究对碳酸钠和碳酸氢钠的化学性质进行了全面的考查,难度较大.

 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案| A. | 2O-2个氧元素 | B. | P2O5-五氧化二磷 | C. | H2-2个氢原子 | D. | Zn-锌分子 |
| A. | 石墨作铅笔芯 | B. | 活性炭吸附冰箱中的异味 | ||
| C. | 天然气作燃料 | D. | 用氢气填充气球 |
| A. | 铁 | B. | 锌 | C. | 钙 | D. | 碘 |
| A. |  向一定体积HCl溶液中滴加NaOH溶液 | |
| B. | 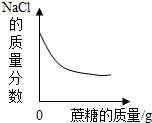 一定温度下,向一定量饱和NaCl溶液中不断加入蔗糖 | |
| C. | 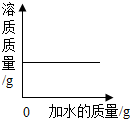 向饱和NaCl溶液中不断加水 | |
| D. |  向CuCl2和H2SO4的混合溶液中加入过量Ba(OH)2溶液 |
| A. | 细铁丝在氧气中燃烧:3Fe+2O2=Fe3O4 | |
| B. | 铁丝与硫酸铜溶液反应:Fe+CuSO4=Cu+FeSO4 | |
| C. | 用稀硫酸与锌反应:Zn+H2SO4=ZnSO4+H2 | |
| D. | 用赤铁矿石(主要成分:Fe2O3)炼铁:CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Fe+CO2 |