题目内容
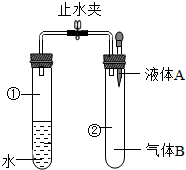 已知水的沸点随压强的减少而降低.现有如图所示实验装置,夹子开始处于关闭状态.将液体A滴入试管②与气体B充分反应后,打开夹子,发现试管①内的水立刻沸腾.A和B最不可能的一种组合是( )
已知水的沸点随压强的减少而降低.现有如图所示实验装置,夹子开始处于关闭状态.将液体A滴入试管②与气体B充分反应后,打开夹子,发现试管①内的水立刻沸腾.A和B最不可能的一种组合是( )| A、A为NaOH溶液,B为CO2气体 |
| B、A为稀H2SO4溶液,B为NH3气体 |
| C、A为AgNO3溶液,B为HCl气体 |
| D、A为CaCl2溶液,B为CO2气体 |
考点:反应现象和本质的联系,酸的化学性质,碱的化学性质
专题:学科交叉型
分析:根据将液体A滴入试管②与气体B充分反应后,打开夹子,发现试管①内的水立刻沸腾,则可知反应的发生使气体减少,压强变小,则由水的沸点随压强的减少而降低,会导致试管①内的水立刻沸腾.
解答:解:A、因氢氧化钠溶液与二氧化碳气体反应生成碳酸钠和水使气体减少,压强变小,试管①内的水会立刻沸腾,故A正确;
B、因稀硫酸与氨气反应生成硫酸铵和水,使气体减少,压强变小,试管①内的水会立刻沸腾,故B正确;
C、因硝酸银溶液与氯化氢气体反应生成氯化银沉淀和硝酸,使气体减少,压强变小,试管①内的水会立刻沸腾,故C正确;
D、因氯化钙溶液与二氧化碳不反应,则不会造成气体的减少,压强不变,所以不能看到试管①内的水会立刻沸腾,故D错误.
故选:D.
B、因稀硫酸与氨气反应生成硫酸铵和水,使气体减少,压强变小,试管①内的水会立刻沸腾,故B正确;
C、因硝酸银溶液与氯化氢气体反应生成氯化银沉淀和硝酸,使气体减少,压强变小,试管①内的水会立刻沸腾,故C正确;
D、因氯化钙溶液与二氧化碳不反应,则不会造成气体的减少,压强不变,所以不能看到试管①内的水会立刻沸腾,故D错误.
故选:D.
点评:本题考查利用反应现象来分析可能发生的反应,利用信息可知判断反应的发生气体减少则压强减小是解答本题的关键,学生应熟悉物质之间的反应来解答.

练习册系列答案
相关题目
将一定量Cu与Cu(OH)2的混合物置于坩埚中充分灼烧,结果所得固体质量恰等于原混合物的质量,则原混合物中铜元素的质量分数为(资料:Cu(OH)2
CuO+H20)( )
| ||
| A、40% | B、25% |
| C、60% | D、80% |
向含有AgNO3,Cu(NO3)2的混合溶液加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,无气体生成.下列说法错误的是( )
| A、滤出的固体中肯定没有Fe |
| B、滤出的固体中肯定含有Ag,Cu |
| C、滤液中可能含有AgNO3 |
| D、滤液中可能含有Cu(NO3)2 |
下列各组变化都属于化学变化的是( )
| A、分离液态空气 |
| B、石油的炼制 |
| C、天然气燃烧 |
| D、石蜡熔化 |
下列生产过程主要发生物理变化的是( )
A、 沼气生产 |
B、 石油分馏 |
C、 转炉炼钢 |
D、 高炉炼铁 |