题目内容
市售“管道通”能使堵塞的管道畅通.小华通过实验对“管道通”中的物质成分进行了探究.
【提出问题】“管道通”中含有什么物质?
【查阅资料】
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道.
(3)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热.例如,铝与盐酸反应的化学方程式是: ,铝与氢氧化钠溶液反应的化学方程式是:2Al+2NaOH+ ═2NaAlO2+3H2↑
【猜想与验证】小华打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
【猜想Ⅰ】白色固体颗粒为氢氧化钠.实验方案如表所示:
【结论】白色固体颗粒为氢氧化钠.
【猜想Ⅱ】银灰色粉末为铝粉.
【实验】取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加 溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰均呈淡蓝色.
【结论】银灰色粉末为铝粉.
【交流与反思】
(1)老师告诉小华,氢氧化钾和氢氧化钠的性质非常相似.因此,要确认猜想Ⅰ是否正确,还需要学习如何检验钠元素的存在.
(2)使用管道通时,先将其中银灰色粉末添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水后立即堵上管道口,管道内迅速发生反应.请写出一个使用“管道通”时的注意事项:避免与皮肤接触(或避免明火,或防止液体喷出,合理答案均可) .
【提出问题】“管道通”中含有什么物质?
【查阅资料】
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污、腐蚀毛发等,可用于疏通管道.
(3)铝粉为银灰色固体,铝与酸、碱溶液都能反应放出氢气,并放出大量热.例如,铝与盐酸反应的化学方程式是:
【猜想与验证】小华打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
【猜想Ⅰ】白色固体颗粒为氢氧化钠.实验方案如表所示:
| 实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿 | |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 | 试管外壁温度明显升高(合理叙述均可) |
| ③向操作②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
【猜想Ⅱ】银灰色粉末为铝粉.
【实验】取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加
【结论】银灰色粉末为铝粉.
【交流与反思】
(1)老师告诉小华,氢氧化钾和氢氧化钠的性质非常相似.因此,要确认猜想Ⅰ是否正确,还需要学习如何检验钠元素的存在.
(2)使用管道通时,先将其中银灰色粉末添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水后立即堵上管道口,管道内迅速发生反应.请写出一个使用“管道通”时的注意事项:避免与皮肤接触(或避免明火,或防止液体喷出,合理答案均可)
考点:实验探究物质的组成成分以及含量,金属的化学性质,碱的化学性质,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【查阅资料】
铝和稀盐酸反应能生成氯化铝和氢气;
化学反应前后,元素的种类不变,原子的种类、总个数不变;
【猜想Ⅰ】
氢氧化钠暴露在空气中时容易潮解,溶于水时能够放出大量的热,氢氧化钠溶液能够溶解毛发等;
【猜想Ⅱ】
铝和稀盐酸、氢氧化钠溶液反应都能够产生氢气;
【交流与反思】
氢氧化钠具有强烈的腐蚀性,氢气与氧气或空气混合达到一定程度时,遇明火会发生爆炸.
铝和稀盐酸反应能生成氯化铝和氢气;
化学反应前后,元素的种类不变,原子的种类、总个数不变;
【猜想Ⅰ】
氢氧化钠暴露在空气中时容易潮解,溶于水时能够放出大量的热,氢氧化钠溶液能够溶解毛发等;
【猜想Ⅱ】
铝和稀盐酸、氢氧化钠溶液反应都能够产生氢气;
【交流与反思】
氢氧化钠具有强烈的腐蚀性,氢气与氧气或空气混合达到一定程度时,遇明火会发生爆炸.
解答:解:【查阅资料】
(3)铝与盐酸反应的化学方程式是:2Al+6HCl═2AlCl3+3H2↑;
根据质量守恒定律可知,铝和氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
故填:2Al+6HCl═2AlCl3+3H2↑;2H2O.
【猜想Ⅰ】实验操作、实验现象如下表所示:
【猜想Ⅱ】
【实验】取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加氢氧化钠溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰均呈淡蓝色.
故填:氢氧化钠.
【交流与反思】
(2)使用管道通时,应该注意:避免与皮肤接触,避免明火,防止液体喷出等.
故填:避免与皮肤接触,避免明火,防止液体喷出等.
(3)铝与盐酸反应的化学方程式是:2Al+6HCl═2AlCl3+3H2↑;
根据质量守恒定律可知,铝和氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
故填:2Al+6HCl═2AlCl3+3H2↑;2H2O.
【猜想Ⅰ】实验操作、实验现象如下表所示:
| 实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿 | 白色固体表面潮湿并逐渐溶解 |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁 | 试管外壁温度明显升高 |
| ③向操作②得到的溶液中放入一段羊毛线,加热一段时间 | 羊毛线逐渐消失 |
【实验】取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加氢氧化钠溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰均呈淡蓝色.
故填:氢氧化钠.
【交流与反思】
(2)使用管道通时,应该注意:避免与皮肤接触,避免明火,防止液体喷出等.
故填:避免与皮肤接触,避免明火,防止液体喷出等.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
分类是学习化学的方法之一,下列各组物质按单质、氧化物、混合物的顺序排列的是( )
| A、钢、氧化镁、空气 |
| B、氮气、氧气、甲烷 |
| C、焊锡、水、复合肥 |
| D、金刚石、冰水、矿泉水 |
下列化学用语表示不正确的是( )
| A、2个氮原子:2N |
| B、钙离子:Ca2+ |
| C、氯化钠:NaCl2 |
| D、碳酸氢钠:NaHCO3 |
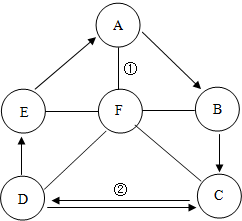 A~F均为初中所学的物质.其中属于碱的是B、C,属于盐的是D、E,其中D是钠盐;胃酸中含有F能帮助消化,A是食品包装袋中常用的干燥剂.其物质间的转化关系如图所示.图中“-”表示两端的物质能发生反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试回答:
A~F均为初中所学的物质.其中属于碱的是B、C,属于盐的是D、E,其中D是钠盐;胃酸中含有F能帮助消化,A是食品包装袋中常用的干燥剂.其物质间的转化关系如图所示.图中“-”表示两端的物质能发生反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试回答: